Drepanocitosis o Enfermedad de células falciformes
Conran N, et al. Newer aspects of the pathophysiology of sickle cell disease vaso-occlusion. Hemoglobin. 2009;33(1):1-16.
Steinberg MH. Sickle cell disease and associated hemoglobinopahies. In: Goldman L, Ausiello D, eds, Cecil Medicine, 23rd ed. Philadelphia, PA; Saunders Elsevier; 2009:1217-26.
Piel FB. et al. Sickle cell disease. N Engl J Med. 2017;376(16):1561-73.
Kalpatthi R, Novelli EM. Measuring success: urility of biomarkers in sickle cell disease clinical trials and care. Hematology Am Soc Hematol Educ Program. 2018. 2018;2018(1):482-92.
Ballas SK, et al. Sickle cell pain: a critical reappraisal. Blood. 2012;120(18(:3647-56.
Habara A, Steinberg MH. Genetic basis of heterogeneity and severity in sickle cell disease. Exp Biol Med (Maywood). 2016:241(7):689-96.
Rees DC, et al. Sickle-cell disease. Lancet. 2010;376(9757):2018-31.
Saraf SL, et al. Differences in the clinical and genotypic presentation of sickle cell disease around the world. Paediatr Respir Rev. 2014;15(1):4-12.
Centers for Disease Control and Prevention. Data & Statistics: Sickle Cell Disease.https://www.cdc.gov/ncbddd/sicklecell/data.html. Último acceso: mayo 2020.
Cancho EJB. et al. Update of the Spanish Registry of Haemoglobinopathies in Children and Adults. Med Clin (Barc). 2020; ;S0025-7753(19)30717-1.
Aliyu ZY, et al. Sickle cell disease and pulmonary hypertension in Africa: a global perspective and review of epidemiology, pathophysiology, and management. Am J hematol. 2008;83:63-70.
Huttle A, et al. Sickle cell disease in Latin America and the United States. Pediatr Blood Cancer. 2015; 62(7):1131-6.
Piel FB, et al. Global burden of sickle cell anaemia in children under five, 2010-2015: modelling based on demographics, excess mortality, interventions. PLoS One. 2013;10(7):1-14.
Puri L, et al. State of the art management of acute vaso-occlusive pain in sickle cell disease. Paediatr Drugs. 2018;20(1):29-42.
Zhang D, et al. Neutrophils, platelets, and inflammatory pathways at the nexus of sickle cell disease pathophysiology. Blood. 2016;127(7):801-9.
Kanter J, Kruse-Jarres R. Management of sickle cell disease from childhood through adulthood. Blood Rev. 2013;27(6):279-87.
Kappelmayer J, Nagy B. The interaction of selectins and PSGL-1 as a key component in thrombus formation and cancer progression. Biomed Res Int. 2017;2017(6138145):1-18.
Chirico EN, Pialoux V. Role of oxidative stress in the pathogenesis of sickle cell disease. IUBMB Life. 2012;64(1):72-80.
Grupo de Eritropatología de la Sociedad Española de Hematología y Hemoterapia. Guía de enfermedad de células falciformes. 2021. Disponible en: https://www.profesionalessanitarios.novartis.es/sites/profesionalessanit.... Último acceso mayo 2022.
Sociedad Española de Hematología y Oncología Pediátricas. Enfermedad de células falciformes. Guía de práctica clínica. 2019. Disponible en: http://www.sehop.org/wp-content/uploads/2019/03/Gu%C3%ADa-SEHOP-Falcifor.... Último acceso mayo 2022.
Piel FB, Steinberg MH, Rees DC. Sickle Cell Disease. N Engl J Med. 2017;376(16):1561-1573.
Grupo de Eritropatología de la Sociedad Española de Hematología y Hemoterapia. Guía de enfermedad de células falciformes. 2021. Disponible en: https://www.profesionalessanitarios.novartis.es/sites/profesionalessanit.... Último acceso mayo 2022.
Grupo de Eritropatología de la Sociedad Española de Hematología y Hemoterapia. Guía de enfermedad de células falciformes. 2021. Disponible en: https://www.profesionalessanitarios.novartis.es/sites/profesionalessanit.... Último acceso mayo 2022.
Sociedad Española de Hematología y Oncología Pediátricas. Enfermedad de células falciformes. Guía de práctica clínica. 2019. Disponible en: http://www.sehop.org/wp-content/uploads/2019/03/Gu%C3%ADa-SEHOP-Falcifor.... Último acceso mayo 2022.
Grupo de Eritropatología de la Sociedad Española de Hematología y Hemoterapia. Guía de enfermedad de células falciformes. 2021. Disponible en: https://www.profesionalessanitarios.novartis.es/sites/profesionalessanit.... Último acceso mayo 2022.
Sociedad Española de Hematología y Oncología Pediátricas. Enfermedad de células falciformes. Guía de práctica clínica. 2019. Disponible en: http://www.sehop.org/wp-content/uploads/2019/03/Gu%C3%ADa-SEHOP-Falcifor.... Último acceso mayo 2022.
Grupo de Eritropatología de la Sociedad Española de Hematología y Hemoterapia. Guía de enfermedad de células falciformes. 2021. Disponible en: https://www.profesionalessanitarios.novartis.es/sites/profesionalessanit.... Último acceso mayo 2022.
Sobre la ECF
Esta información va destinada únicamente a profesionales sanitarios; si no lo eres, visita anemiafalciforme.es
Trastorno genético complejo
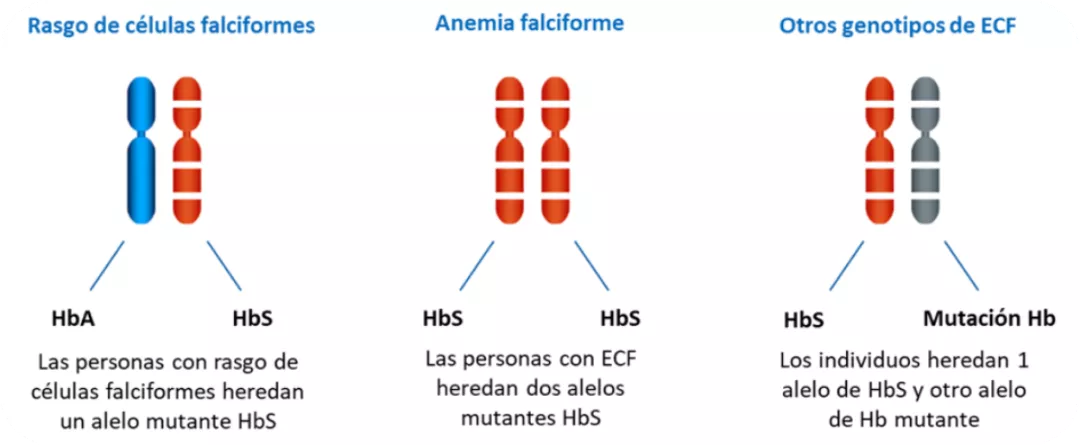
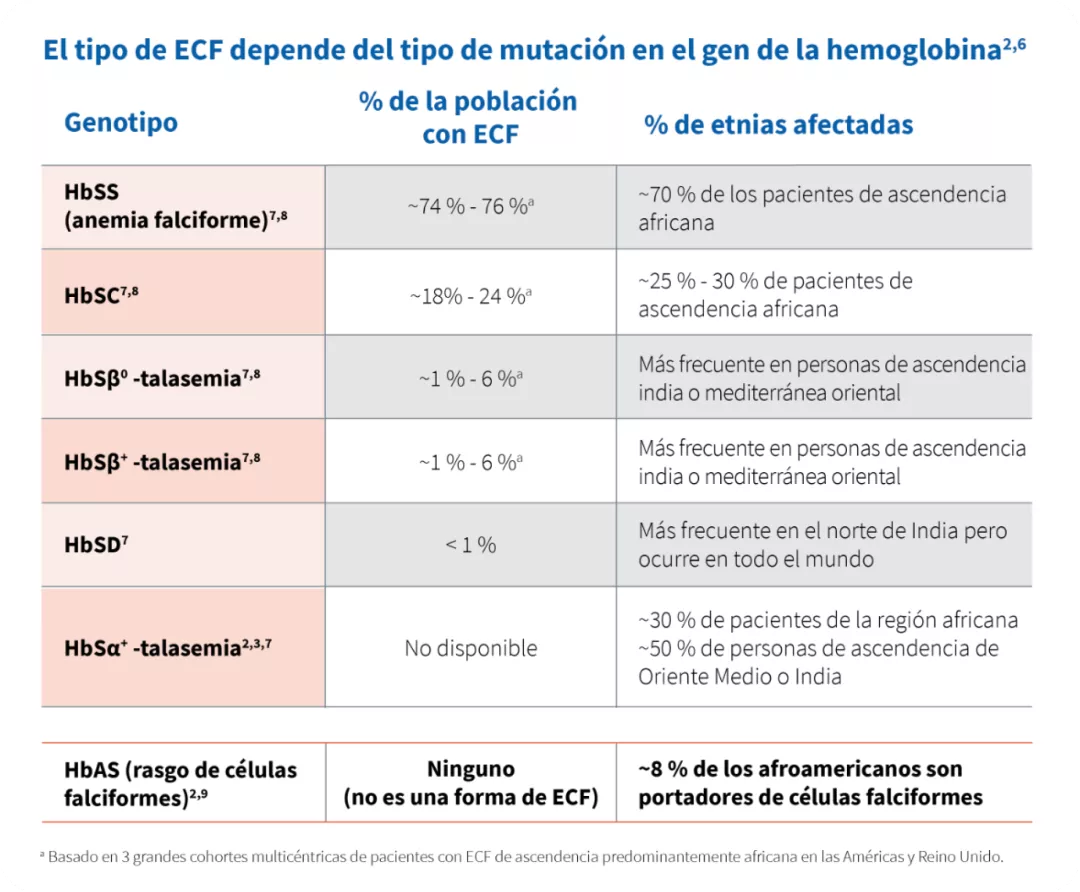
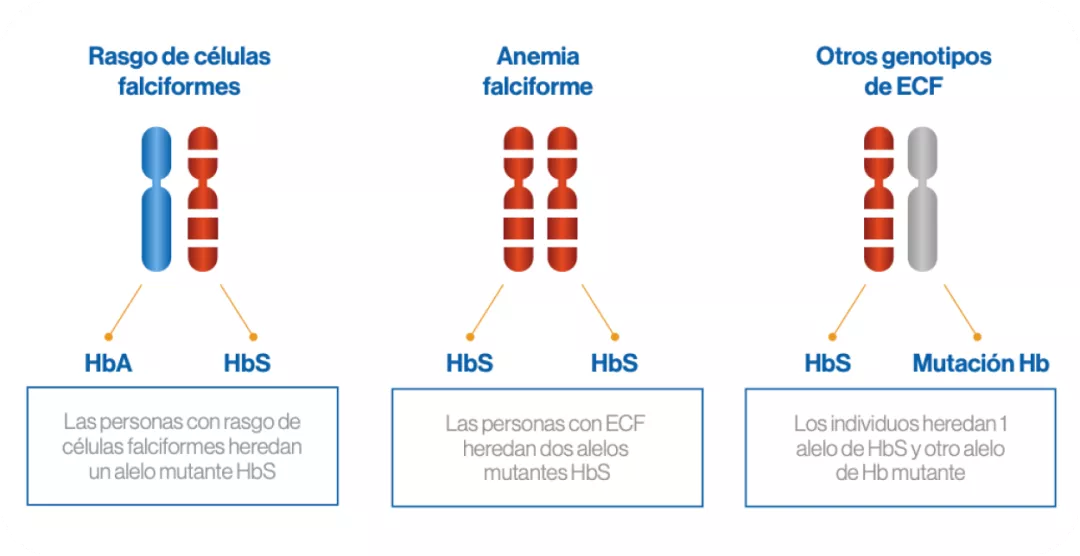
Genotipos comunes
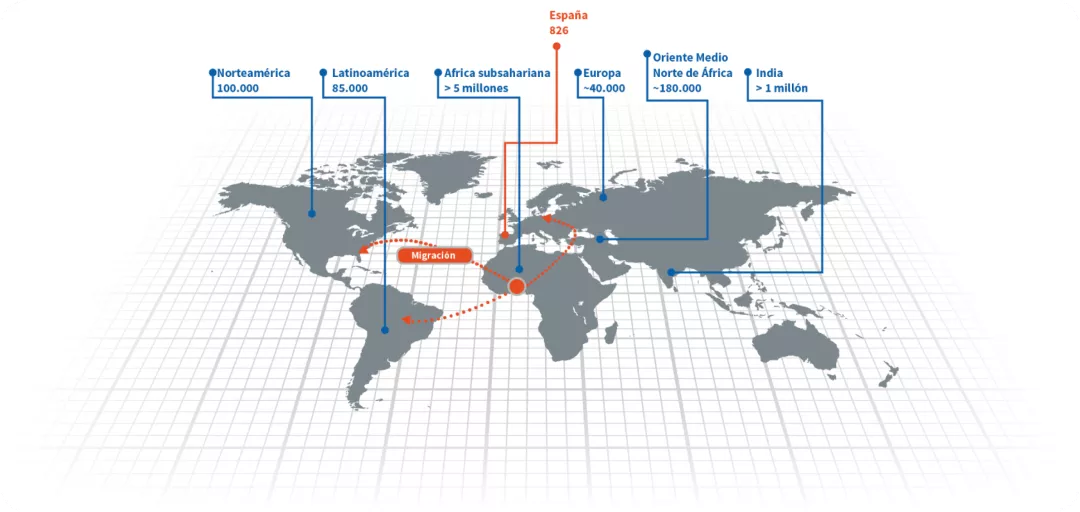
En 2050 se espera que el número de personas nacidas con ECF crezca un 30% en todo el mundo.13
Mecanismos subyacentes
Referencias
Concepto e incidencia
Concepto
Incidencia
Referencias
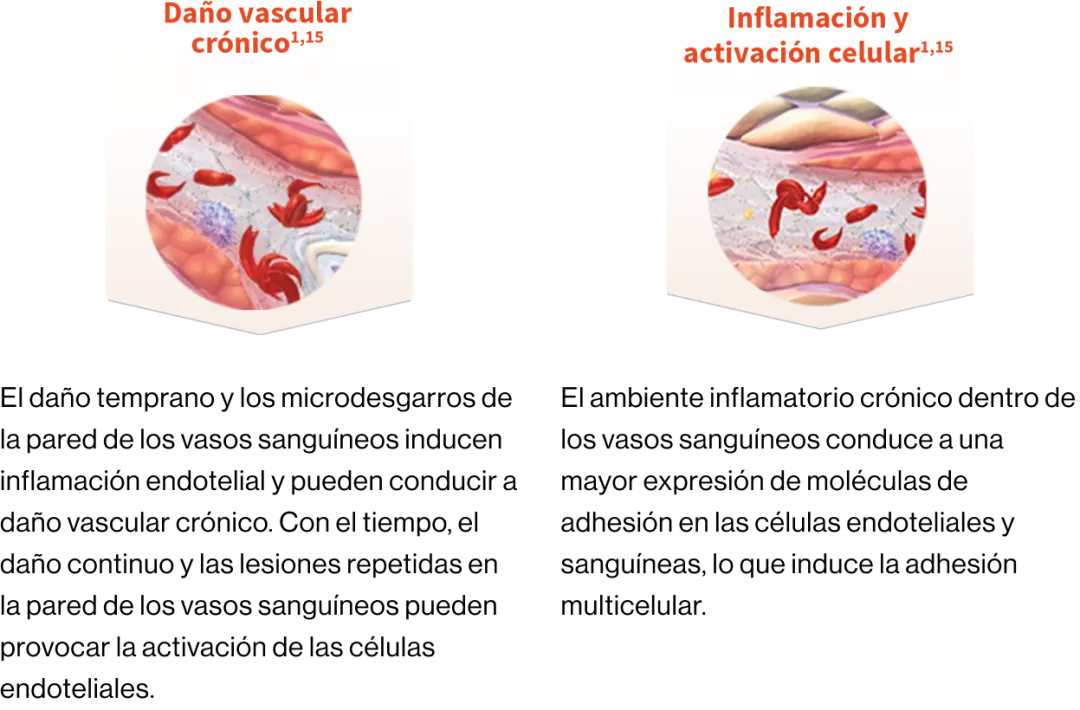
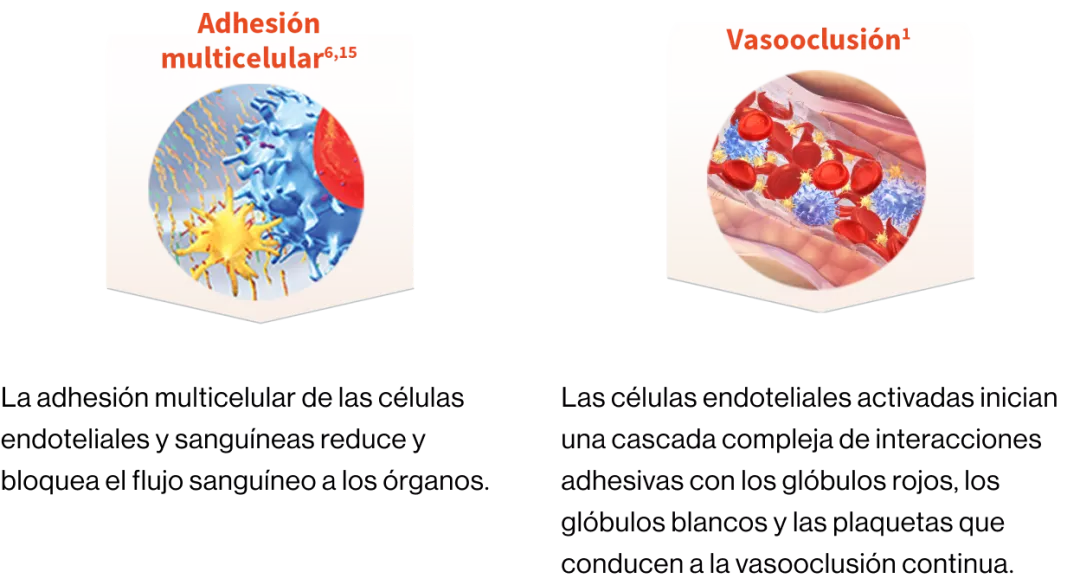
Fisiopatología
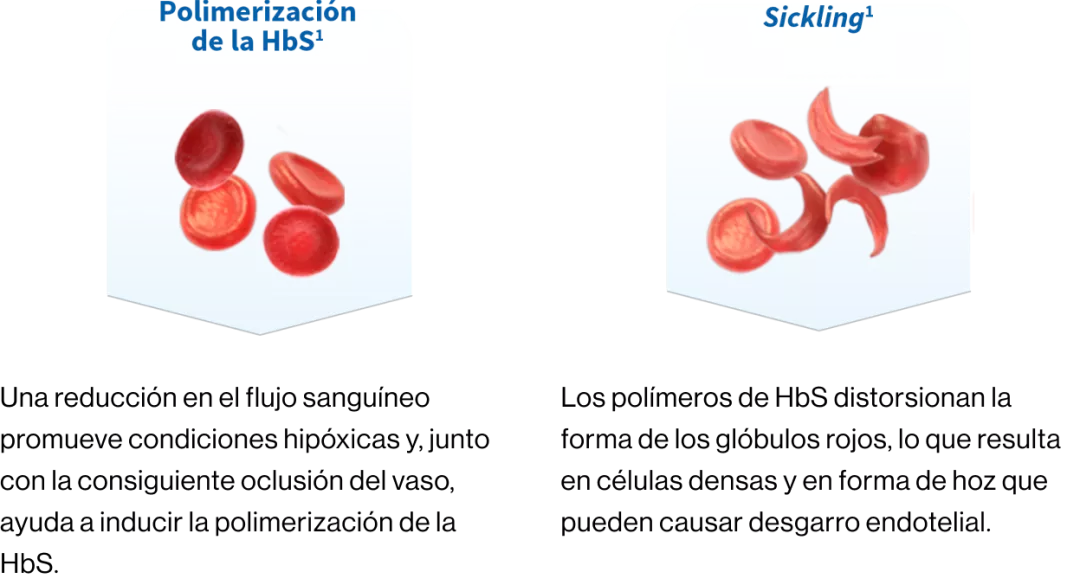
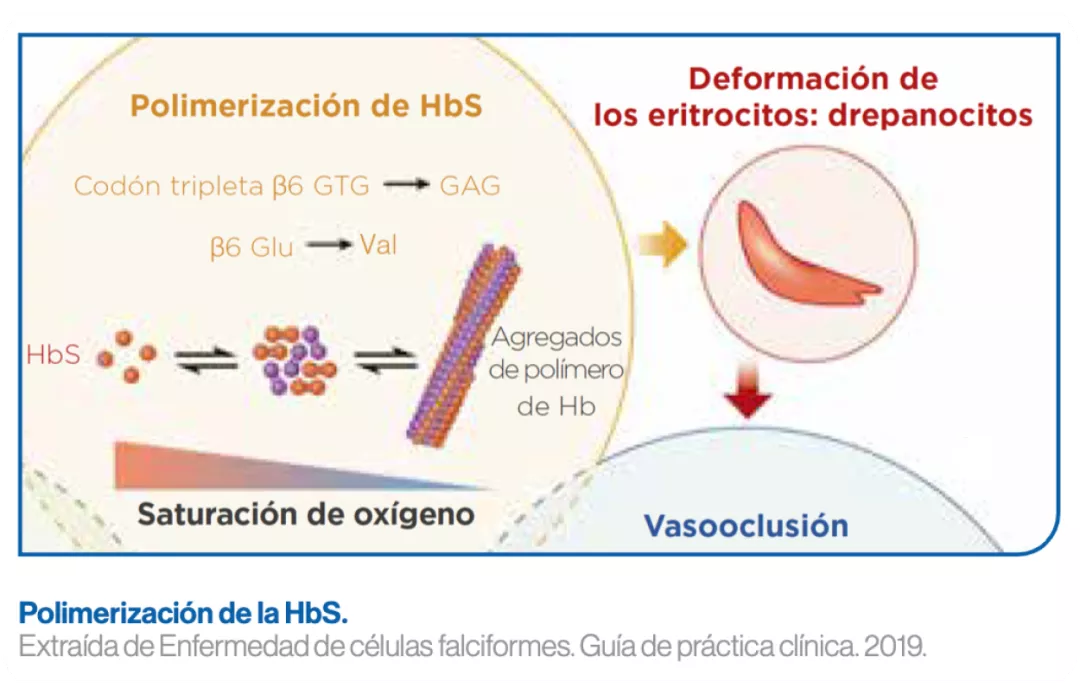
Polimerización de la hemoglobina
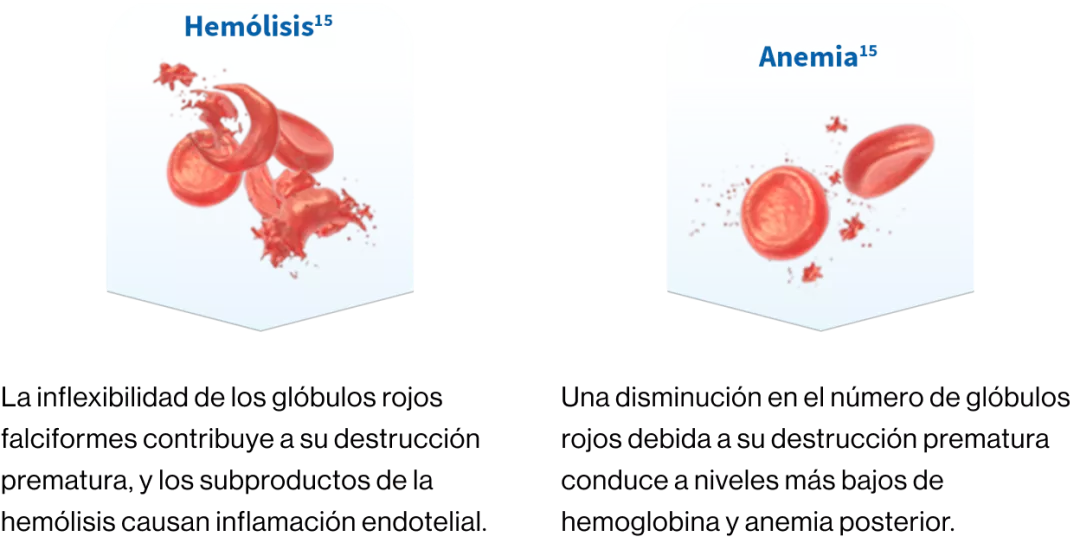
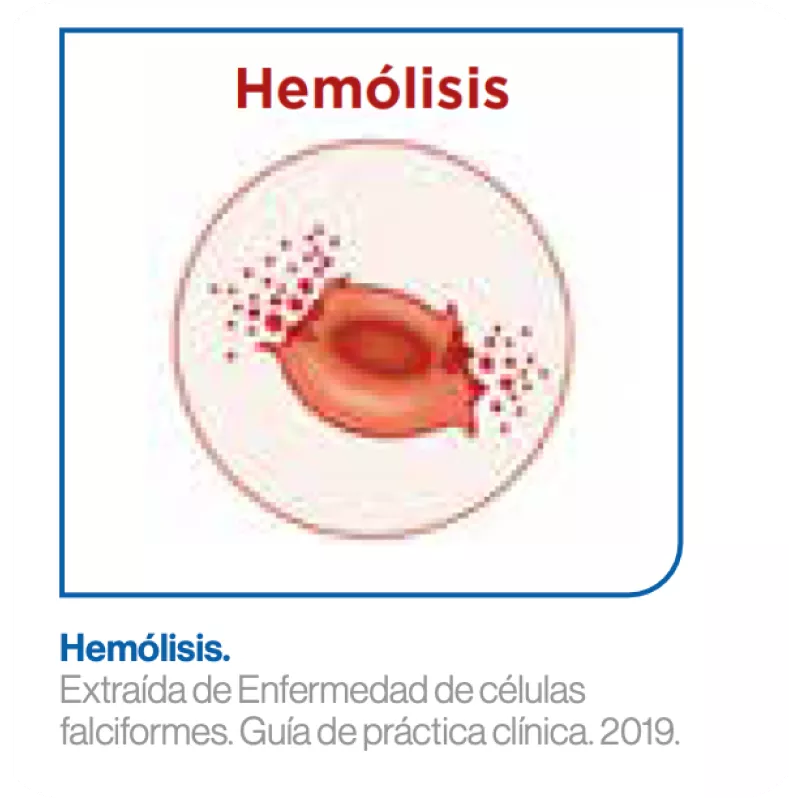
Hemólisis
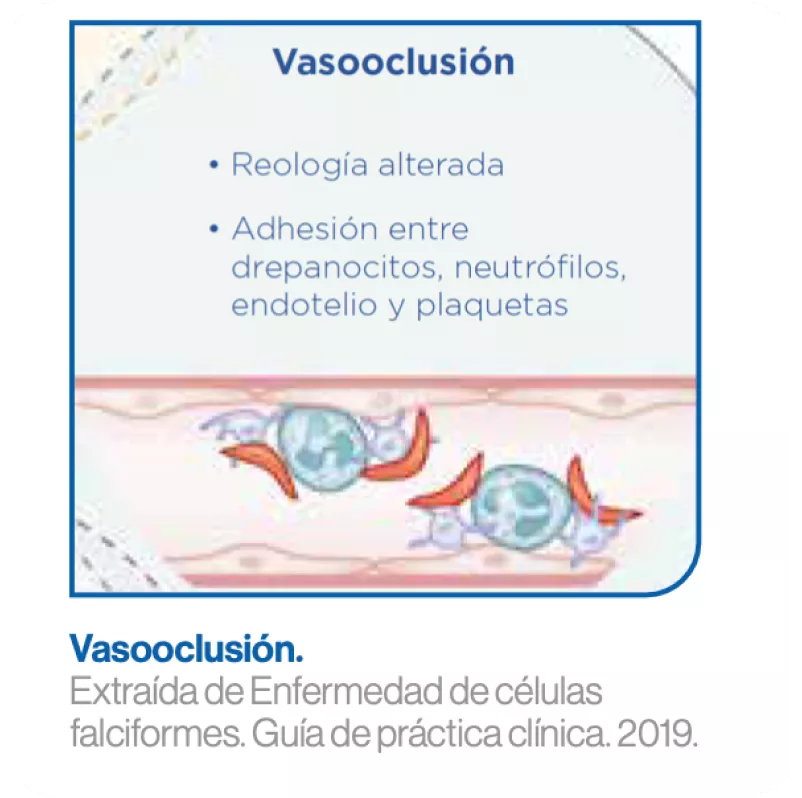
Crisis vasooclusivas
Inflamación crónica y daño endotelial
Referencia
Cribado neonatal
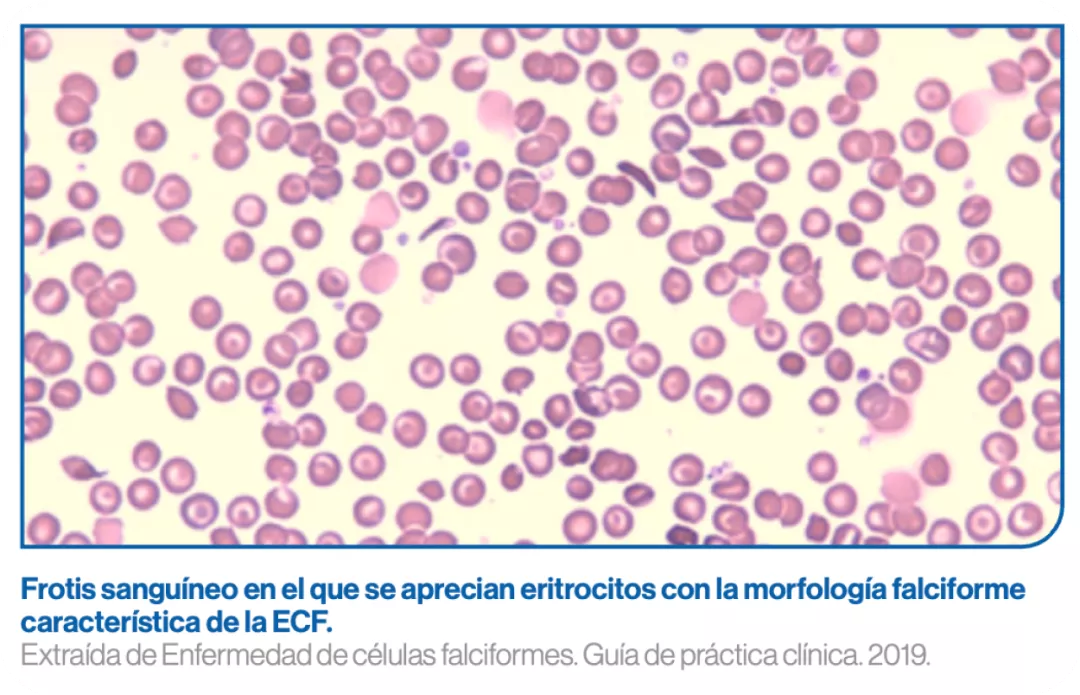
Datos hematimétricos y extensión de sangre periférica
Diagnóstico preciso
Referencias
Referencia
Pronóstico y clasificación
Referencias
Grupo de Eritropatología de la Sociedad Española de Hematología y Hemoterapia. Guía de enfermedad de células falciformes. 2021. Disponible en: https://www.profesionalessanitarios.novartis.es/sites/profesionalessanit.... Último acceso mayo 2022.
Sociedad Española de Hematología y Oncología Pediátricas. Enfermedad de células falciformes. Guía de práctica clínica. 2019. Disponible en: http://www.sehop.org/wp-content/uploads/2019/03/Gu%C3%ADa-SEHOP-Falcifor.... Último acceso mayo 2022.
Sociedad Española de Hematología y Oncología Pediátricas. Enfermedad de células falciformes. Guía de práctica clínica. 2019. Disponible en: http://www.sehop.org/wp-content/uploads/2019/03/Gu%C3%ADa-SEHOP-Falcifor.... Último acceso mayo 2022.
Profilaxis infecciosa
Hemoterapia
Hidroxiurea
Nuevos tratamientos
Referencias
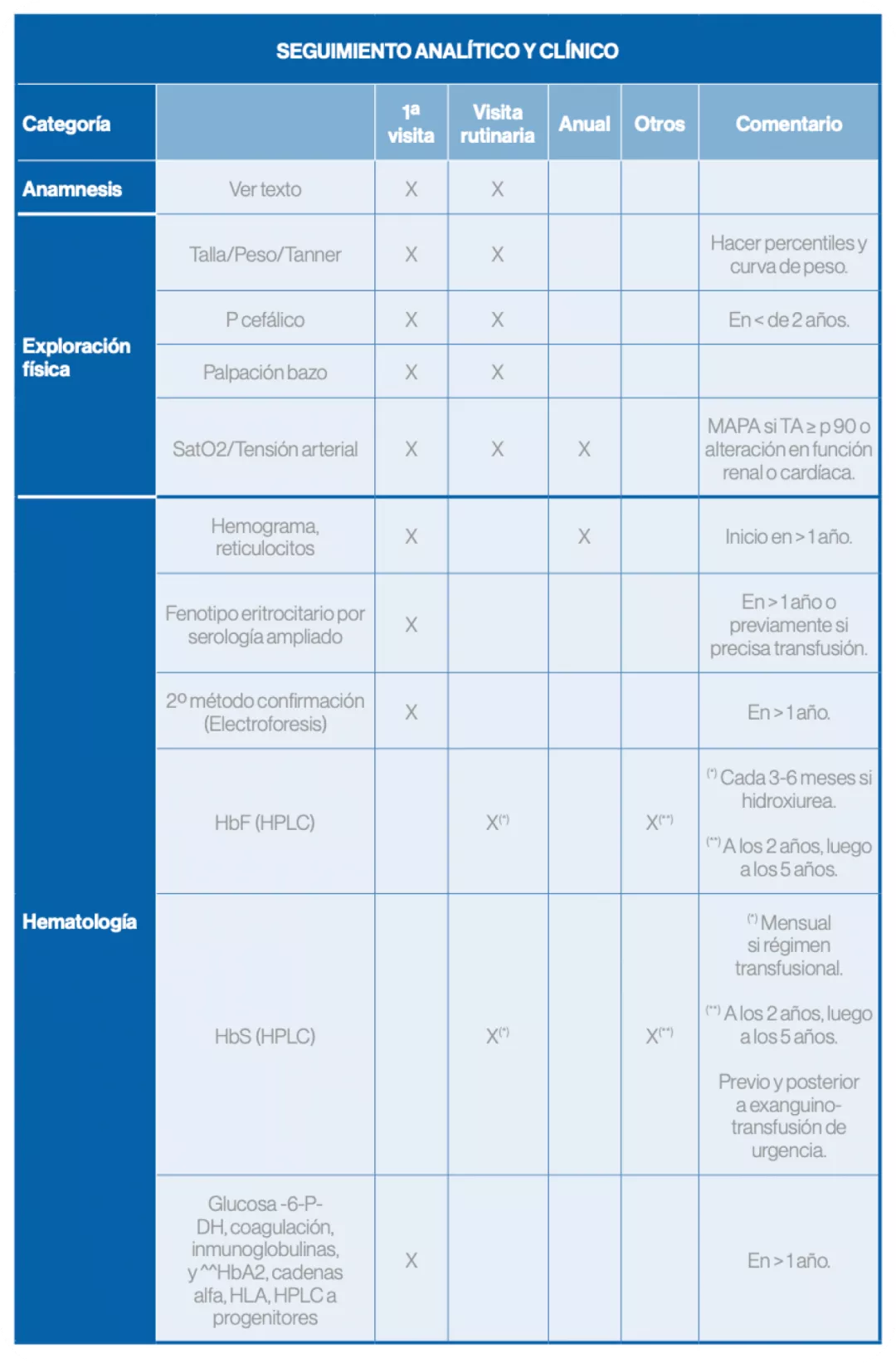
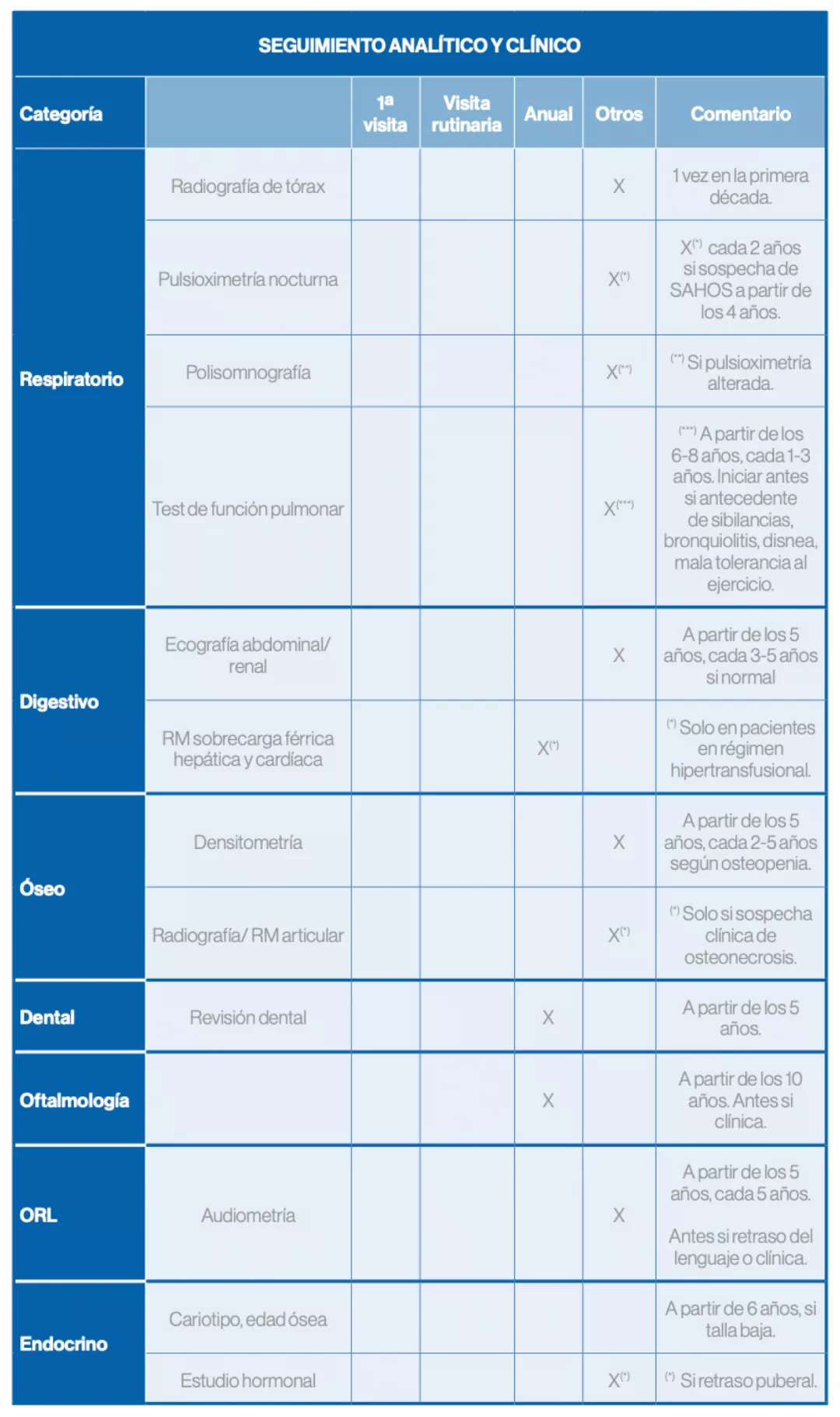
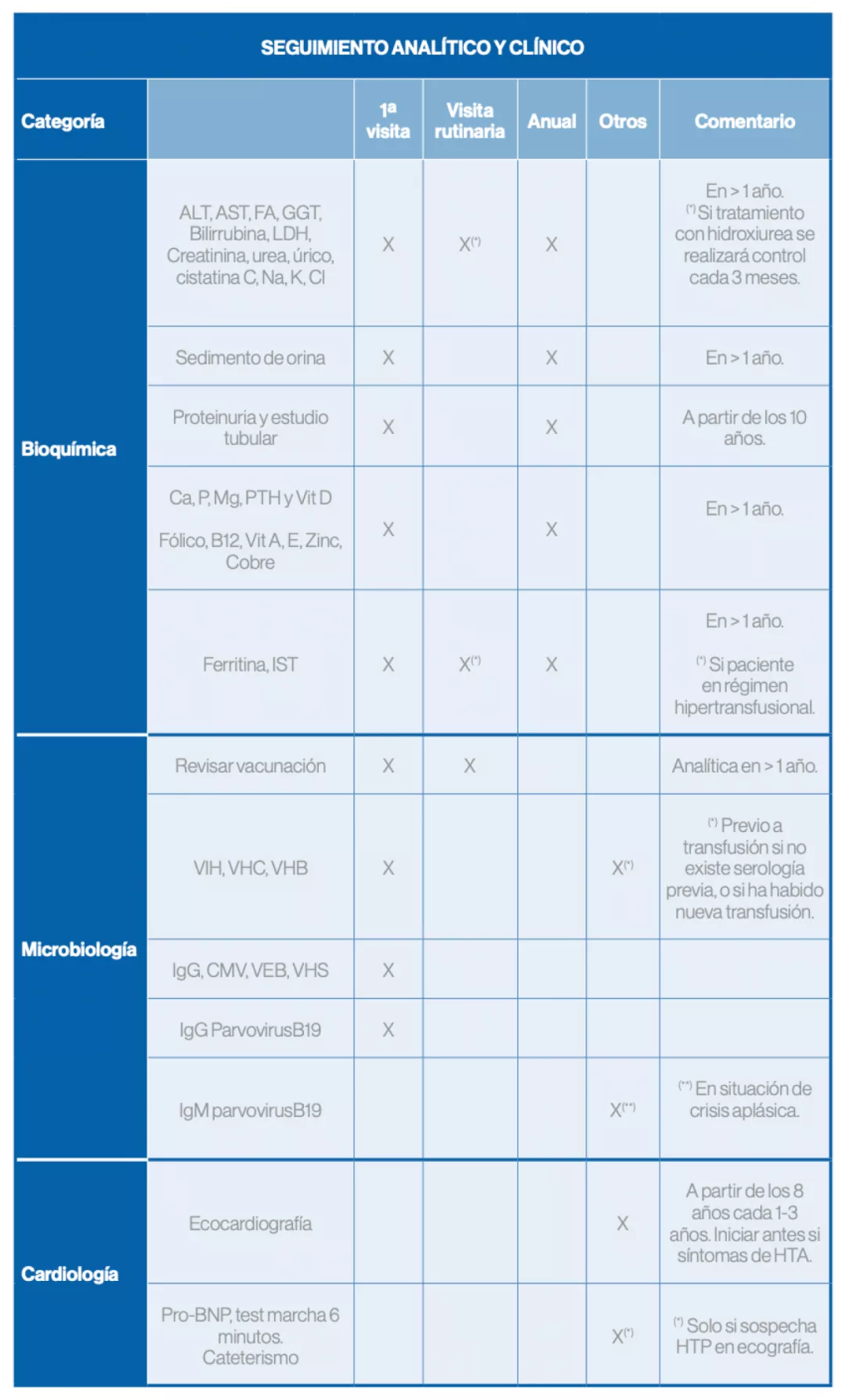
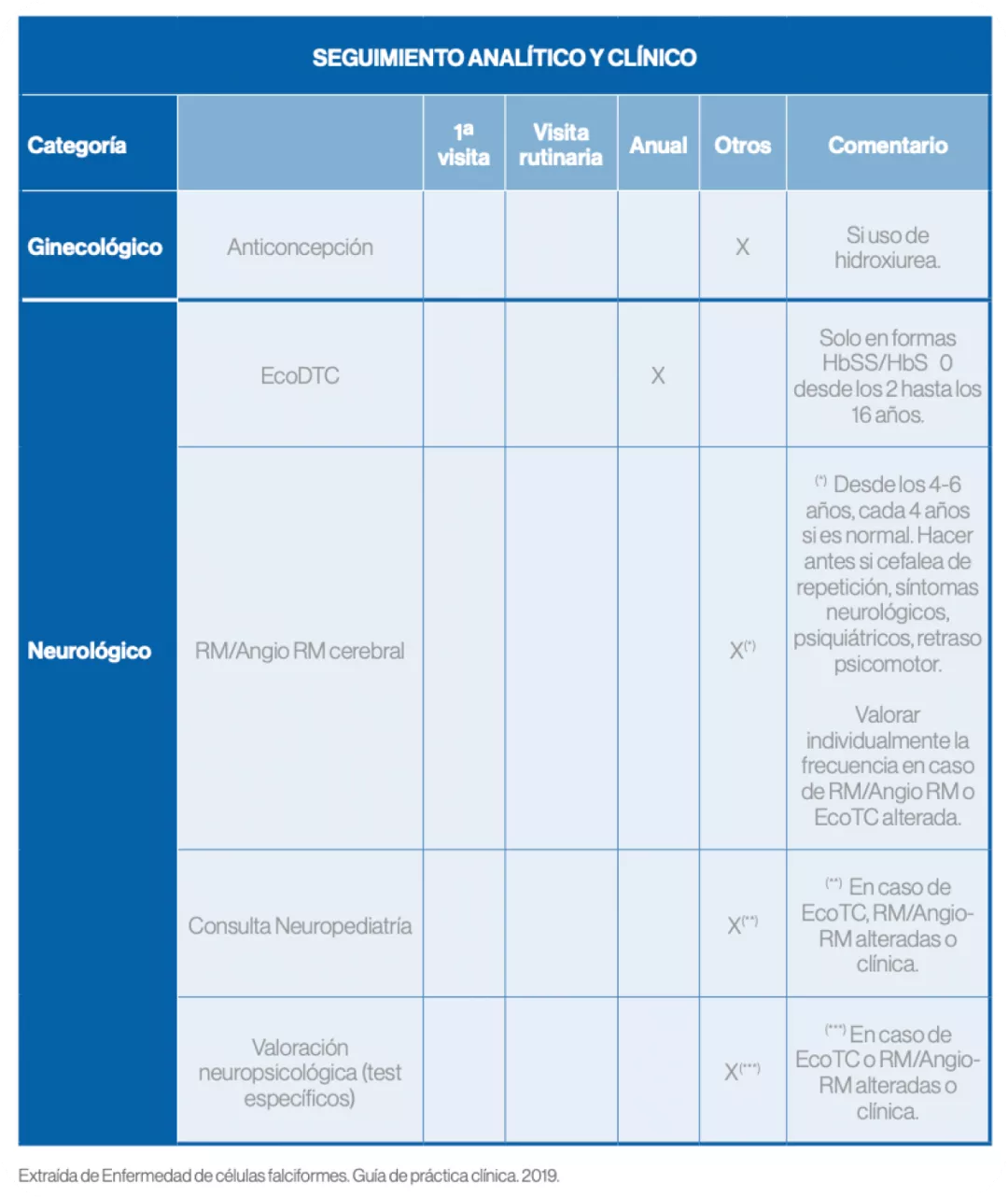
Seguimiento