Dette nettstedet er kun for helsepersonell som lege, offentlig godkjent sykepleier og farmasøyt
Om Tafinlar & Mekinist
Føflekkreft med spredning for BRAF-positive
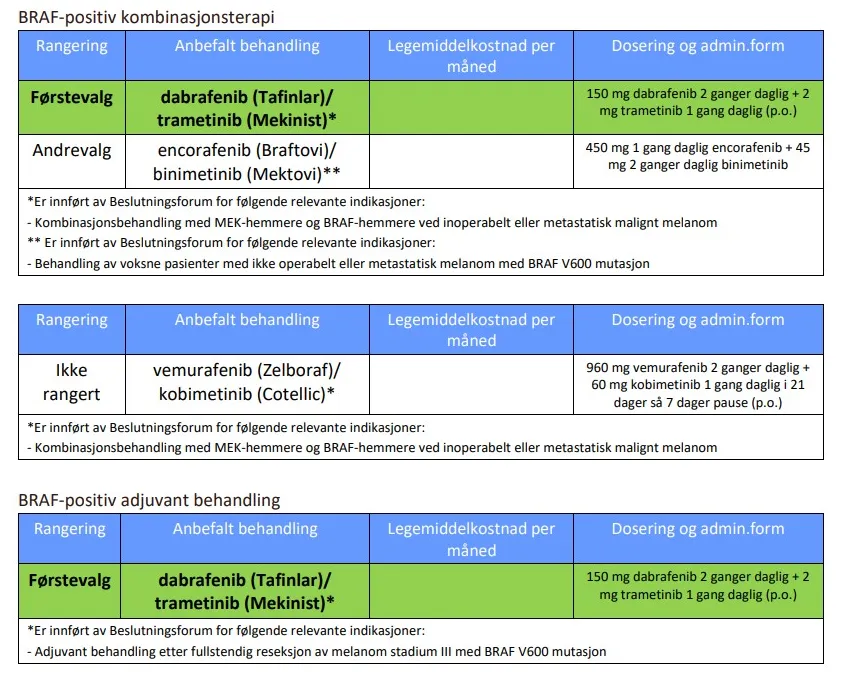
Bildet er hentet fra Sykehusinnkjøp HF. Anbefalinger fra Spesialistgruppe for onkologi. Oslo: Sykehusinnkjøp HF; 2025 Sep 17 [sist lest 2025 Sep 18].
Les hele 2507 avtalen her
Tafinlar (dabrafenib) & Mekinist (trametinib)
Indikasjon 1,2
Melanom: Behandling, som monoterapi eller i kombinasjon av dabrafenib og trametinib, av voksne med inoperabelt eller metastaserende melanom med en BRAF V600-mutasjon.1,2
Adjuvant behandling av melanom: Adjuvant behandling, i kombinasjonav dabrafenib og trametinib, av voksne med stadium III melanom med BRAF V600-mutasjon, etter fullstendig reseksjon.1,2
Ikke-småcellet lungekreft (NSCLC): Behandling, med dabrafenib og trametinib i kombinasjon, av voksne med avansert NSCLC med en BRAF V600-mutasjon.1,2
Viktige egenskaper
Forbedret overlevelsesrate: Kliniske studier har vist betydelige forbedringer i både total overlevelse og progresjonsfri overlevelse hos pasienter behandlet med Tafinlar® og Mekinist®.1,2
Bivirkninger
De vanligste bivirkningene (forekomst ≥ 20 %) for dabrafenib i kombinasjon med trametinib var pyreksi, fatigue, kvalme, frysninger, hodepine, diaré, oppkast, artralgi og utslett. 1-2
Virkningsmekanisme
Tafinlar er en hemmer av RAF-kinase, som reduserer virkningen av BRAF. Mekinist, derimot, hemmer aktiveringen og effekten av MEK1 og MEK2. Ved å virke på disse to punktene i MAPK/ERK-signalveien, hemmer Tafinlar og Mekinist samtidig både MEK og RAF. Dette fører til en kombinert nedregulering av denne signalveien. 1-2
Dosering og administrasjon
Behandling bør startes og overvåkes av lege med erfaring med kreftlegemidler. Før behandlingsstart skal BRAF V600-mutasjonsstatus bekreftes med validert test. Voksne: Anbefalt dose, som monoterapi eller i kombinasjon med trametinib, er 150 mg (2 kapsler à 75 mg) 2 ganger daglig (tilsv. daglig dose på 300 mg). Anbefalt dose av trametinib, i kombinasjon med dabrafenib, er 2 mg 1 gang daglig. Vedvarende behandling anbefales inntil nytte/effekt opphører eller uakseptabel toksisitet utvikles. Ved adjuvant behandling av melanom bør behandlingsperioden være 12 måneder, med mindre tilbakefall av sykdom eller uakseptabel toksisitet oppstår.1-2
Dosejusteringer
Ved bivirkninger kan dosereduksjon eller midlertidig/permanent seponering være nødvendig. Dosejustering eller midlertidig avbrudd anbefales ikke ved bivirkninger som kutant plateepitelkarsinom (cuSCC) eller ved nytt primært melanom. Ved feber se Forsiktighetsregler. Anbefalte dosereduksjoner:
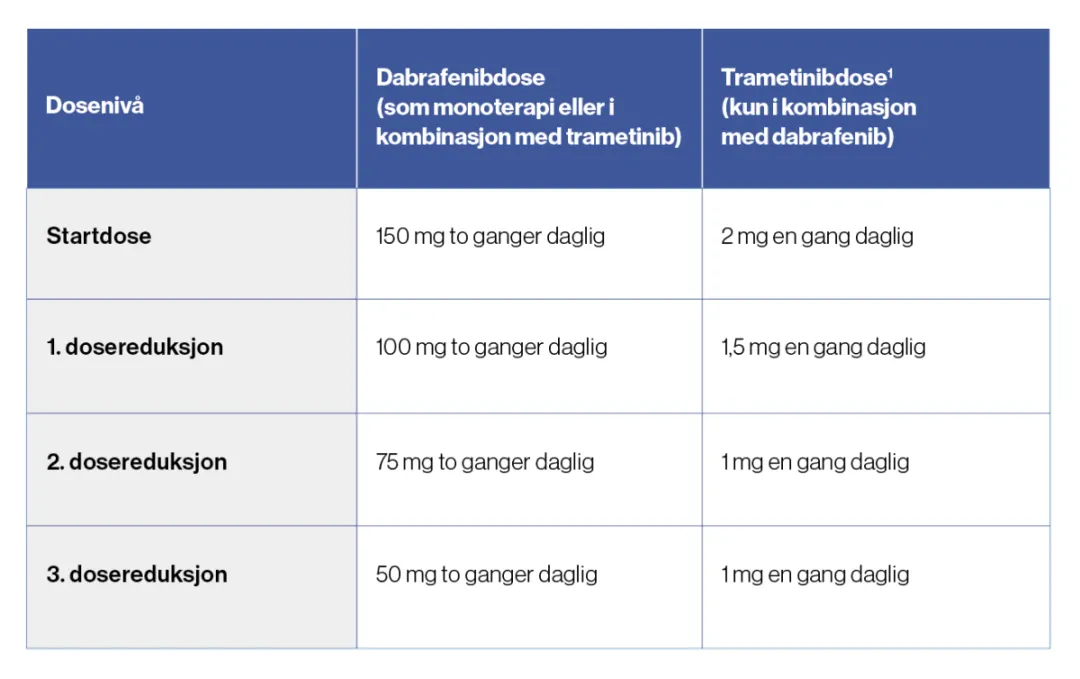
Se preparatomtalen til trametinib for instruksjoner vedrørende monoterapibehandling med trametinib. Dabrafenibdoser (enten som monoterapi eller i kombinasjon med trametinib) <50 mg 2 ganger daglig er ikke anbefalt. Trametinibdoser (i kombinasjon med dabrafenib) <1 mg 1 gang daglig er ikke anbefalt. 1-2
Referanser:
SPC Mekinist avsnitt. 4.1, 4.2, 5.1
SPC Tafinlar avsnitt. 4.1, 4.2, 5.1
Sikkerhetsinformasjon
Indikasjoner: Melanom: Behandling, som monoterapi eller i kombinasjon dabrafenib og trametinib, av voksne med inoperabel eller metastaserende melanom med en BRAF V600-mutasjon. Adjuvant behandling av melanom: Adjuvant behandling, i kombinasjon av dabrafenib og trametinib, av voksne med stadium III melanom med BRAF V600-mutasjon, etter fullstendig reseksjon. Ikke-småcellet lungekreft (NSCLC): Behandling, i kombinasjon av dabrafenib og trametinib, av voksne med avansert NSCLC med BRAF V600-mutasjon.
Vanligste bivirkninger: Pyreksi, fatigue, kvalme, frysninger, hodepine, diaré, oppkast, artralgi og utslett.
Kontraindikasjoner: Overfølsomhet for innholdsstoffene.
Dosering: 150 mg (to 75 mg kapsler) dabrafenib to ganger daglig (som tilsvarer en daglig dose på 300 mg). Anbefalt dose av trametinib er 2 mg én gang daglig.
Forsiktighetsregler: Forsiktighet utvises hos pasienter med moderat til alvorlig nedsatt leverfunksjon, alvorlig nedsatt nyrefunksjon, svekket venstre ventrikkelfunksjon, hos eldre >65 år, ved samtidig bruk av antikoagulasjonsbehandling og annen økt risiko for blødning, kjent risiko for gastrointestinal perforasjon f.eks. ved metastaser til tarm og divertikulitt. Ved tidligere retinal veneokklusjon (RVO) er behandling ikke anbefalt og ved interstitiell lungesykdom (ILD) og lungebetennelse bør behandling midlertidig holdes tilbake. Tilfeller av bilateral panuveitt eller bilateral iridosyklitt, som tyder på Vogt Koyanagi-Harada-syndrom, har blitt rapportert.
Listepris: Tafinlar: 50 mg 28stk 11 107,40 kr, 50 mg 120stk 46 302,00 kr, 75 mg 28stk 16 596,10 kr, 75 mg 120stk 69 387,90 kr. Mekinist: 0,5 mg 30stk 32 941,6 kr, 2 mg 30stk 98 752,40 kr. Reseptgruppe: C. Refusjon: H-resept, vilkår 216.
For mer informasjon, se felleskatalogen for Tafinlar og Mekinist.
