Dette nettstedet er kun for helsepersonell som lege, offentlig godkjent sykepleier og farmasøyt
Medisinsk vitenskapelig informasjon
COMBI-AD: Tafinlar og Mekinist som adjuvant behandling etter fullstendig reseksjon av melanom stadium III med BRAF V600 mutasjon
Studiedesign og primære endepunkt
I denne dobbeltblindede, placebokontrollerte, fase III studien ble 870 pasienter med fullstendig resektert stadium III melanom med BRAF V600E eller V600K mutasjoner randomisert 1:1 for å motta enten kombinasjonsbehandling (dabrafenib 150 mg to ganger daglig og trametinib 2 mg én gang daglig) eller to placeboer i en periode på 12 måneder. Det primære endepunktet var tilbakefallsfri overlevelse (RFS). Sekundære endepunkter inkluderte total overlevelse (OS), fravær av tilbakefall (FFR), fjernmetastasfri overlevelse (DMFS)1,4

Effektdata
Inklusjonskriterier2,4
- Pasienter med stadium III (stadium IIIA [lymfeknutemetastase > 1 mm], IIIB eller IIIC) kutant melanom med en BRAF V600 E/K-mutasjon, etter fullstendig reseksjon.
- Fullstendig lymfadenektomi innen 12 uker i forkant av randomisering
- Ingen systemisk kreftbehandling inkludert ingen tidligere strålebehandling.1,2
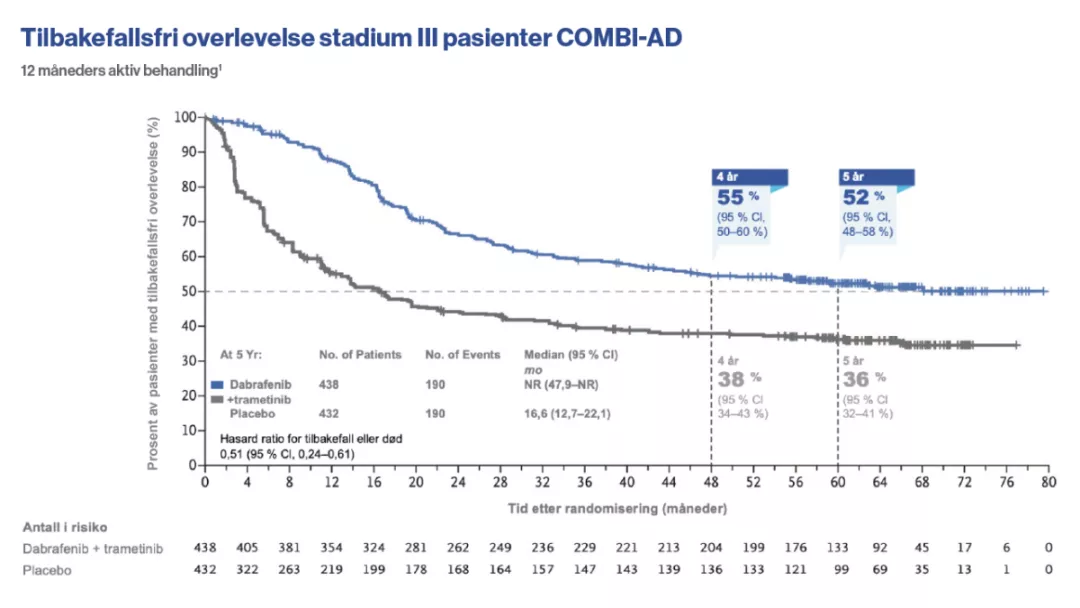
Resultater ved 5-års oppfølging
Ved 5-års oppfølgingen var median tilbakefallsfri overlevelse (RFS) fortsatt ikke nådd (NR) (95 % Kl, 47,9-NR) sammenlignet med 16.6 måneder (95 % CI, 12,7-22,1) for placebo i COMBI-AD (HR, 0,51; 95 % CI, 0,42-0,61)1
I primæranalysen var median RFS NR i Tafinlar og Mekinist gruppen (95 % CI, 44,5-ikke estimert) og 16,6 måneder i placebogruppen (95 % CI, 12,7-22,1); (HR, 0,47; 95 % CI, 0,39-0,58); P<,0001)3,4
Median oppfølgingstid for oppdatert analyse var 60 måneder i Tafinlar og Mekinist behandlingsarmen og 58 måneder for placebogruppen1
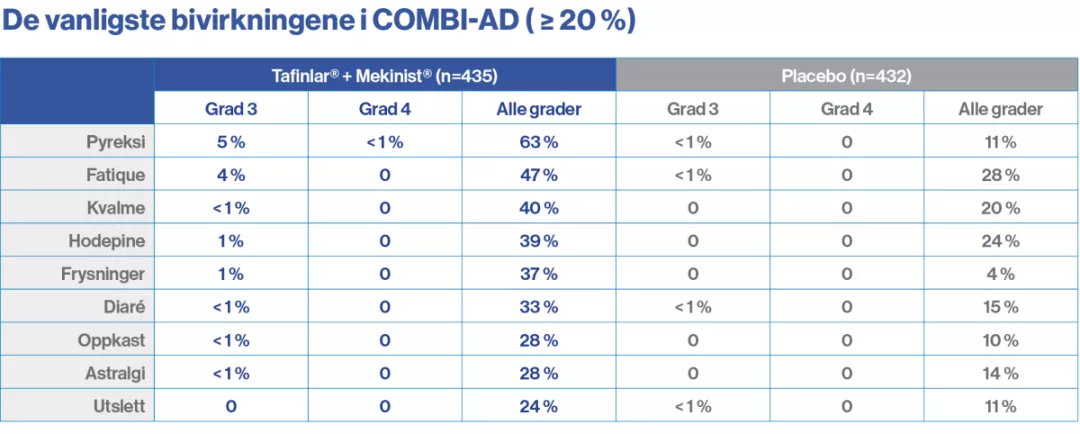
Resultater ved endelige analyser med nærmere 10-års oppfølging:5
Median oppfølgingstid var totalt 8,33 år fra endelige analyser av COMBI-AD-studien.
Total overlevelse
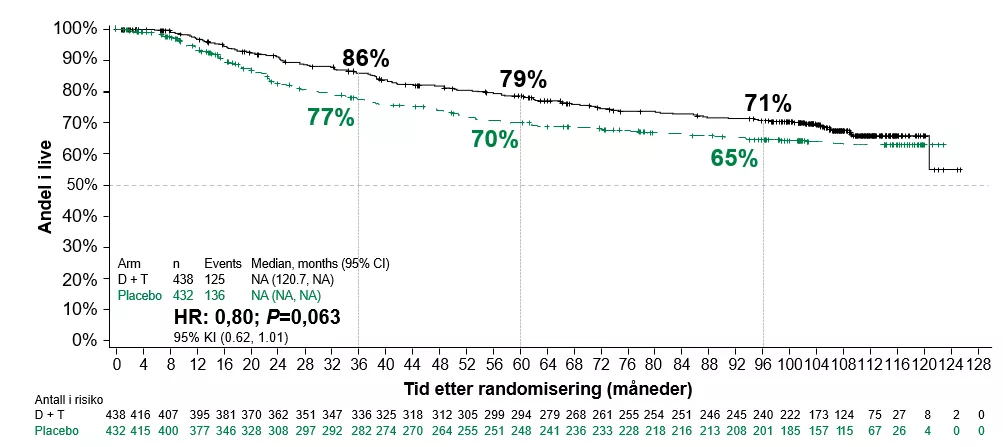
Kaplan–Meier-estimater for total overlevelse favoriserte Tafinlar og Mekinist over placebo, selv om fordelen ikke var signifikant (HR for død, 0,80; 95 % KI, 0,62- 1,01; P = 0,06 ved stratifisert log-rank test). En overlevelsesfordel ble sett på tvers av flere forhåndsdefinerte subgrupper, inkludert de 792 pasientene med melanom med en BRAF V600E-mutasjon (HR for død, 0,75; 95 % KI, 0,58 til 0,96).
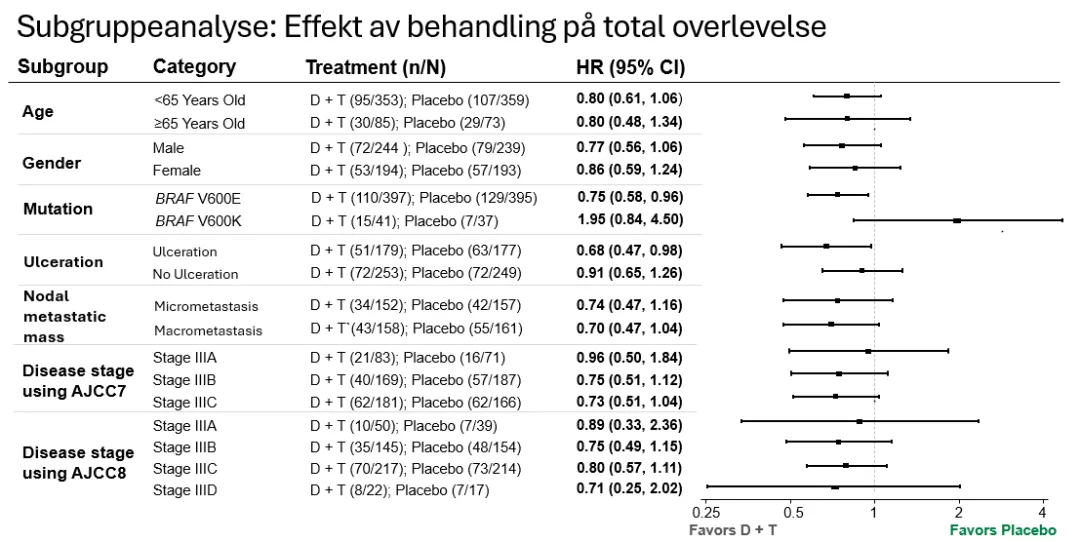
Effekt av behandling på subgruppenivå antydet fordeler med hensyn til total overlevelse ved bruk av Tafinlar og Mekinist sammenlignet med placebo i de fleste subgrupper, og melanom med en BRAF V600E-mutasjon, pasienter med primær tumorulcerasjon og pasienter med makrometastaser så ut til å ha gå mest i favør av behandling med Tafinlar og Mekinist sammenlignet med placebo.
Subgruppeanalyse: Effekt av behanding på total overlevelse ved BRAF V600 E/K-mutasjoner
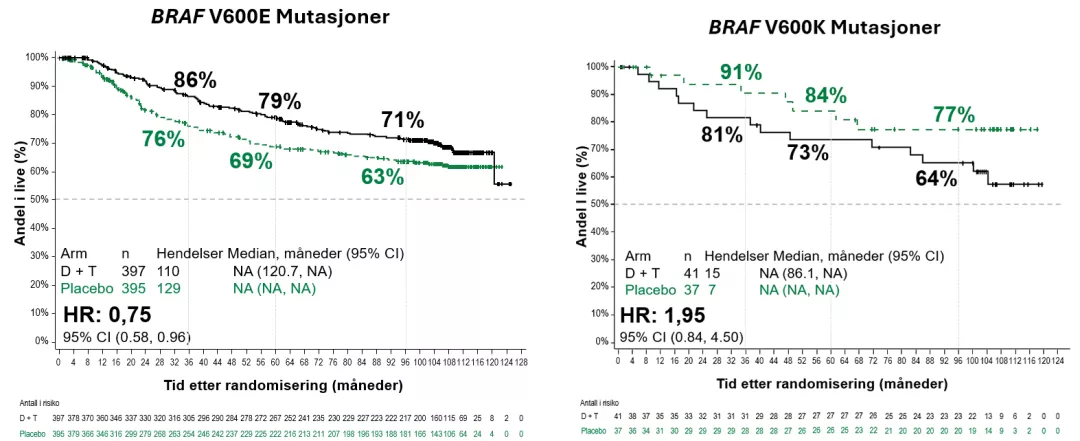
Resultatene for total overlevelse for pasientene med BRAF V600E-mutasjon (HR, 0,75; 95 % KI, 0,58 til 0,96) behandlet med Tafinlar og Mekinist var tilnærmet de i den totale studiepopulasjonen. For pasientene med BRAF V600K-mutasjon var imidlertid reversert med HR for død, 1,95; 95 % KI, 0,84 til 4,50.
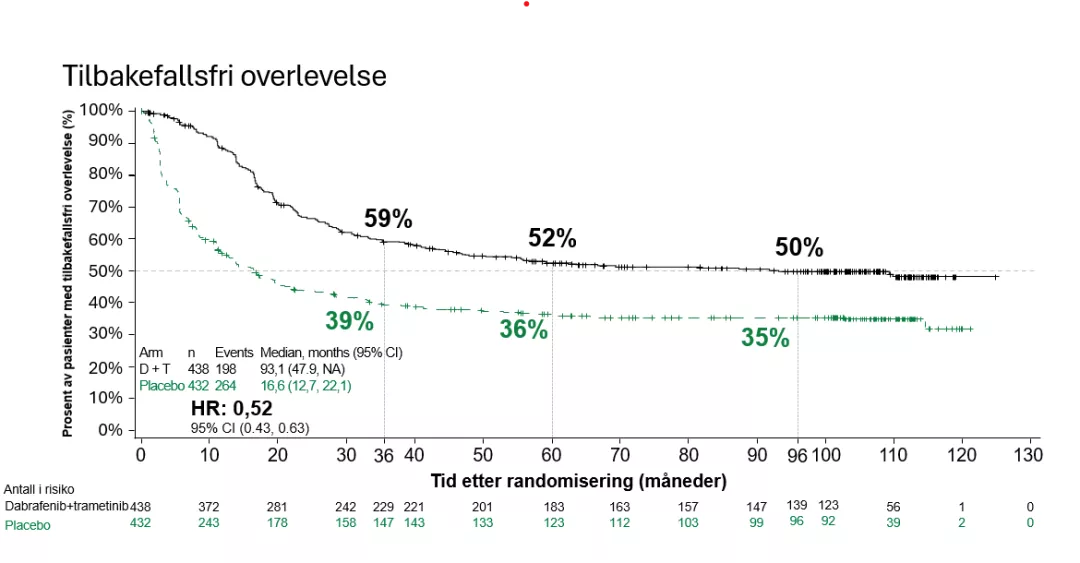
Tilbakefallsfri overlevelse viste en fordel ved Tafinlar og Mekinist over placebo (HR for tilbakefall eller død, 0,52; 95 % KI, 0,43 til 0,63). Det samme gjorde fjernmetastasefri overlevelse (HR for fjernmetastase eller død, 0,56; 95 % KI, 0,44 til 0,71). Analysen viste at resultatene var uavhengig av BRAF V600E- og K-mutasjoner.
Sikkerhetsdata fra nærmere 10-års oppfølging i COMBI-AD:5
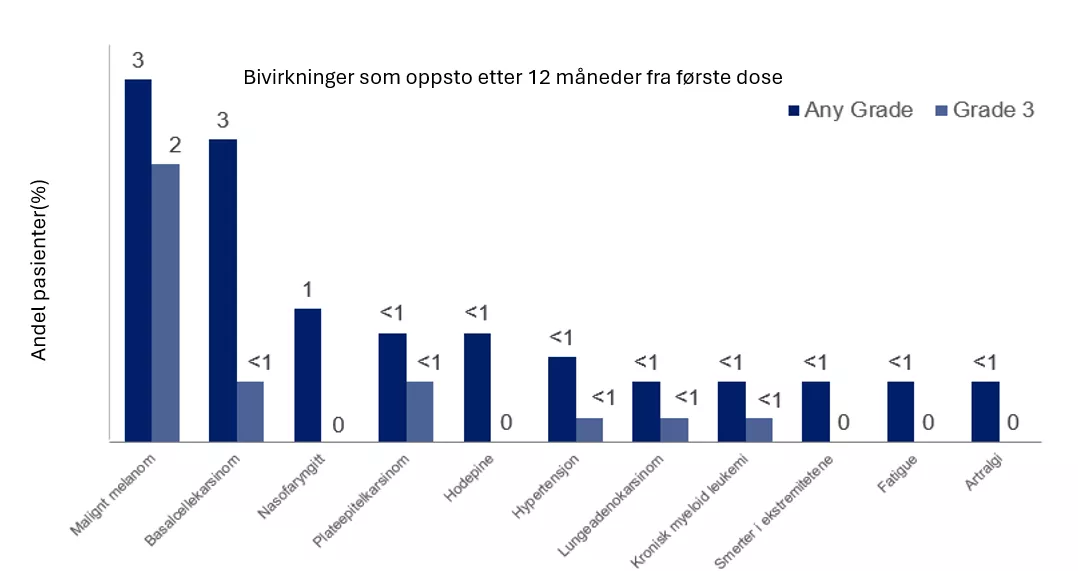
Det ble ikke observert nye sikkerhetssignaler etter 12 måneder fra første dose i oppfølgingsstudien på nærmere 10 år. Totalt ble bivirkninger rapportert for 422 pasienter (97 %) i kombinasjonsbehandlingsgruppen og 381 pasienter (88 %) i placebogruppen. Alvorlige bivirkninger ble rapportert for henholdsvis 178 (41 %) i kombinasjonsbehandlingsgruppe og 58 (13 %) i placebogruppen.
Referanser:
1: Dummer R et al. Five-Year Analysis of Adjuvant Dabrafenib plus Trametinib in Stage III Melanoma. N Engl J Med. 2020 Sept 17: 383:1139-1148. doi: 10.1056/NEJMoa2005493.
2: Long GV, Hauschild A, Santinami M et al. Adjuvant Dabrafenib plus Trametinib in Stage III BRAF-Mutated Melanoma. New England Journal of Medicine. 2017, 377: 1813-23
3: Tafinlar SPC avsnitt 5.1
4: Mekinist SPC avsnitt 5.1
5: Long GV et al. Final Results for Adjuvant Dafrafenib plus Trametinib in Stage III Melanoma. N Engl J Med 2024; 391: 1709-20. doi: 10.1056/NEJMoa2404139
Sikkerhetsinformasjon
Indikasjoner: Melanom: Behandling, som monoterapi eller i kombinasjon dabrafenib og trametinib, av voksne med inoperabel eller metastaserende melanom med en BRAF V600-mutasjon. Adjuvant behandling av melanom: Adjuvant behandling, i kombinasjon av dabrafenib og trametinib, av voksne med stadium III melanom med BRAF V600-mutasjon, etter fullstendig reseksjon. Ikke-småcellet lungekreft (NSCLC): Behandling, i kombinasjon av dabrafenib og trametinib, av voksne med avansert NSCLC med BRAF V600-mutasjon.
Vanligste bivirkninger: Pyreksi, fatigue, kvalme, frysninger, hodepine, diaré, oppkast, artralgi og utslett.
Kontraindikasjoner: Overfølsomhet for innholdsstoffene.
Dosering: 150 mg (to 75 mg kapsler) dabrafenib to ganger daglig (som tilsvarer en daglig dose på 300 mg). Anbefalt dose av trametinib er 2 mg én gang daglig.
Forsiktighetsregler: Forsiktighet utvises hos pasienter med moderat til alvorlig nedsatt leverfunksjon, alvorlig nedsatt nyrefunksjon, svekket venstre ventrikkelfunksjon, hos eldre >65 år, ved samtidig bruk av antikoagulasjonsbehandling og annen økt risiko for blødning, kjent risiko for gastrointestinal perforasjon f.eks. ved metastaser til tarm og divertikulitt. Ved tidligere retinal veneokklusjon (RVO) er behandling ikke anbefalt og ved interstitiell lungesykdom (ILD) og lungebetennelse bør behandling midlertidig holdes tilbake. Tilfeller av bilateral panuveitt eller bilateral iridosyklitt, som tyder på Vogt Koyanagi-Harada-syndrom, har blitt rapportert.
Listepris: Tafinlar: 50 mg 28stk 11 107,40 kr, 50 mg 120stk 46 302,00 kr, 75 mg 28stk 16 596,10 kr, 75 mg 120stk 69 387,90 kr. Mekinist: 0,5 mg 30stk 32 941,6 kr, 2 mg 30stk 98 752,40 kr. Reseptgruppe: C. Refusjon: H-resept, vilkår 216.
For mer informasjon, se felleskatalogen for Tafinlar og Mekinist.
