
Коррекция нежелательных явлений на фоне терапии комбинацией дабрафениб + траметиниб
Оглавление
Основные признаки типичных НЯ на фоне таргетной терапии комбинацией дабрафениб + траметиниб
Офтальмологическая токсичность
Терапия комбинацией дабрафениб + траметиниб у пациентов с меланомой характеризуется в целом удовлетворительным профилем безопасности. Несмотря на то, что нежелательные явления (НЯ) любой степени развиваются у 98% пациентов, принимающих комбинацию дабрафениб + траметиниб, большинство из них относятся к 1–2 степени, контролируемы и не вызывают осложнений [1–3]. Можно не допустить развития осложнений, если вовремя распознать и скорректировать НЯ.
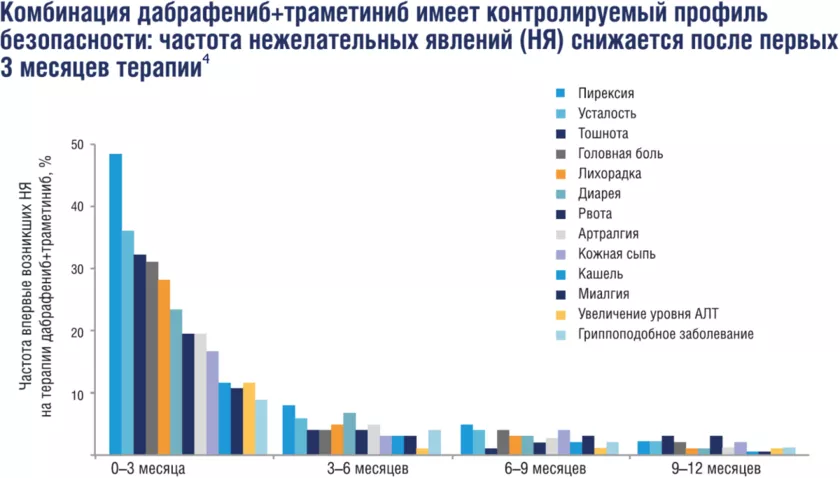
Сокращение.
АЛТ — аланинаминотрансфераза.
Основные признаки типичных НЯ на фоне таргетной терапии комбинацией дабрафениб + траметиниб
Некоторые НЯ довольно редкие, и важно не пропустить их признаки при осмотре пациента.
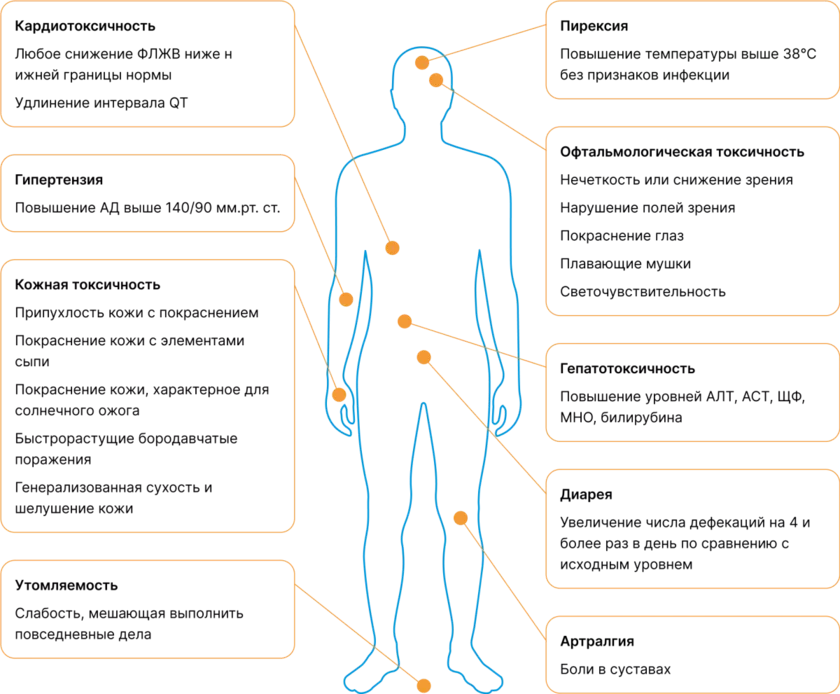
Пирексия
Пирексия — наиболее частое НЯ на фоне лечения комбинацией дабрафениб + траметиниб.


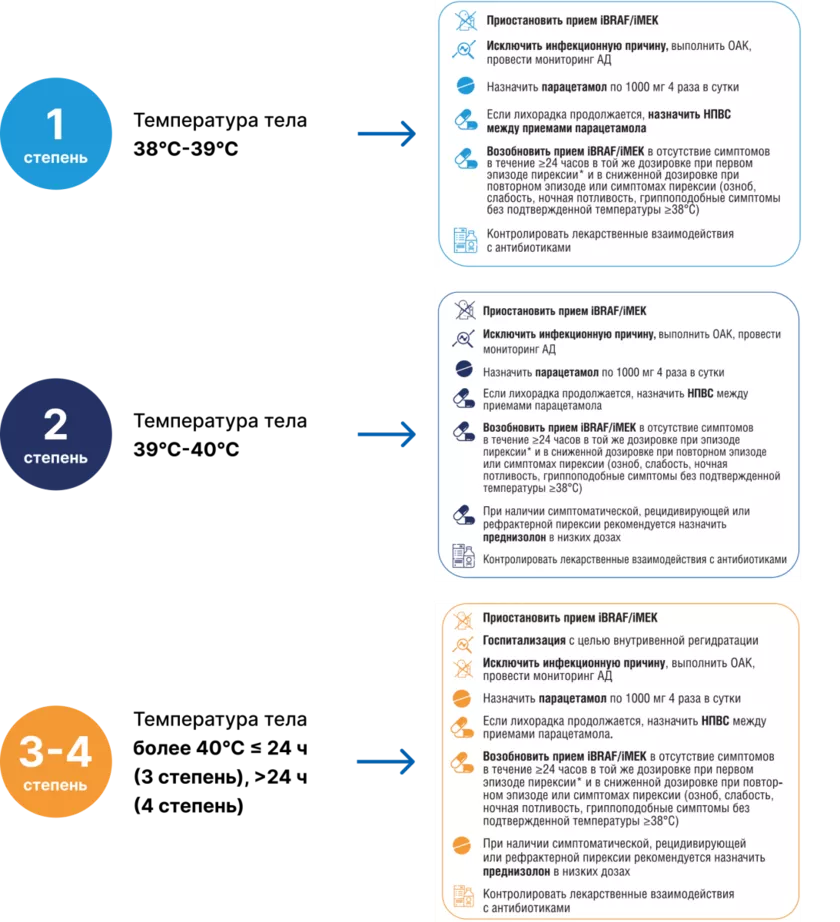
Алгоритм действий при развитии пирексии [17]
Пирексия — наиболее частое НЯ на фоне лечения комбинацией дабрафениб + траметиниб.
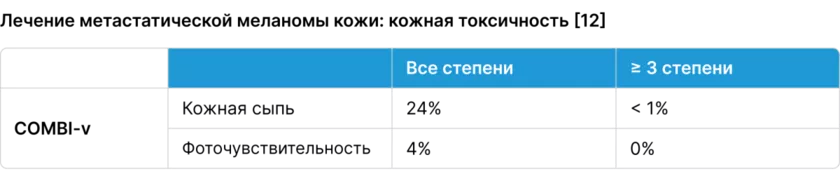
Кожная токсичность
Ингибиторы BRAF могут запустить ненормальную пролиферацию клеток кожи — парадоксальная активация нормального каскада MAPK/ERK в нормальных кератиноцитах, что обуславливает кожную токсичность [18, 19].
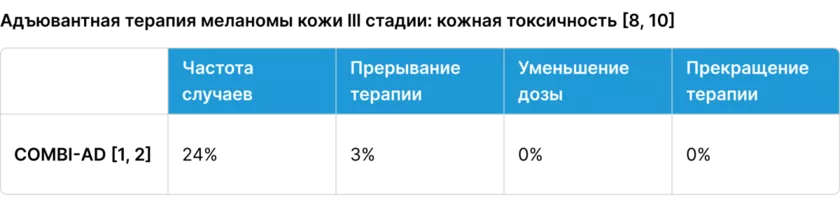
Алгоритм действий при развитии кожной токсичности

Алгоритм действий при макулярных/папулезных или перифолликулярных высыпаниях [17]
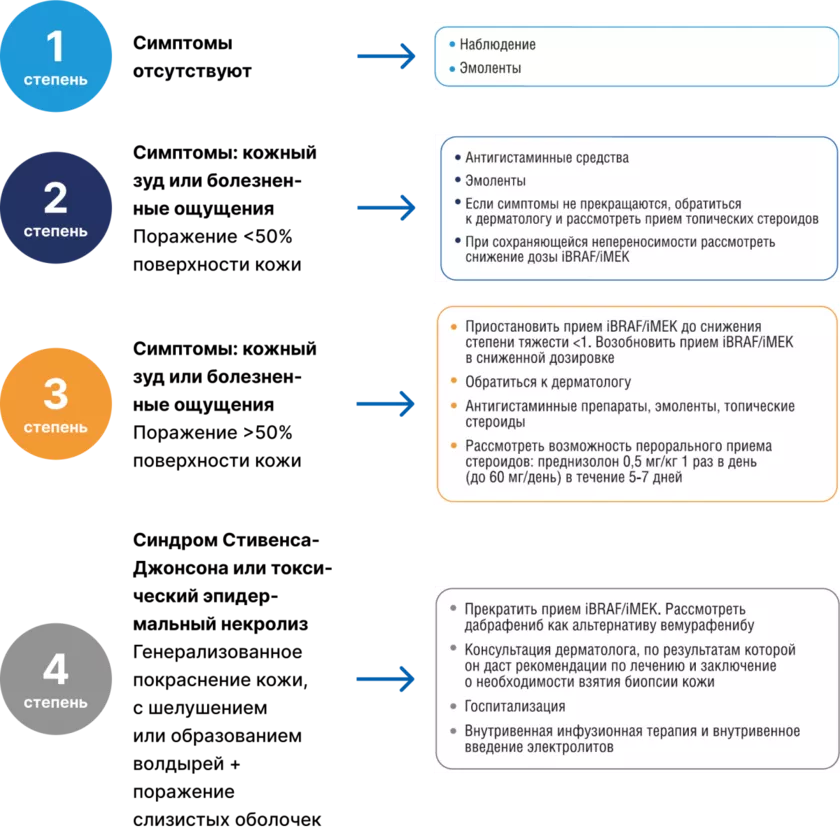
Офтальмологическая токсичность
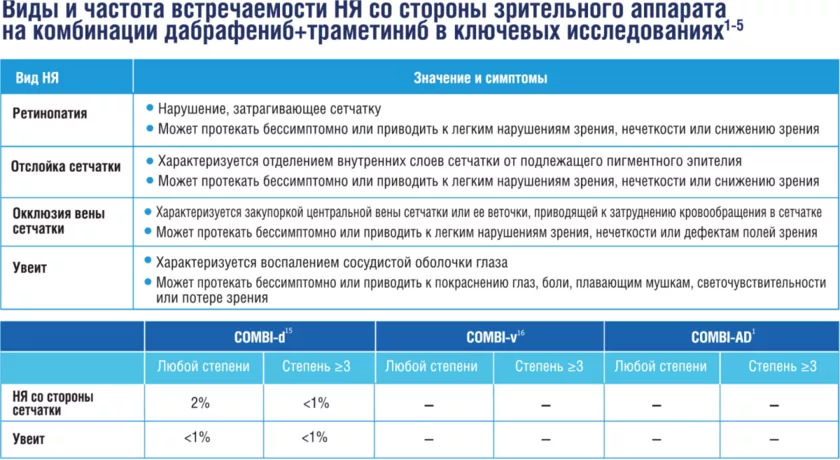
Алгоритм действий при офтальмологической токсичности [17]
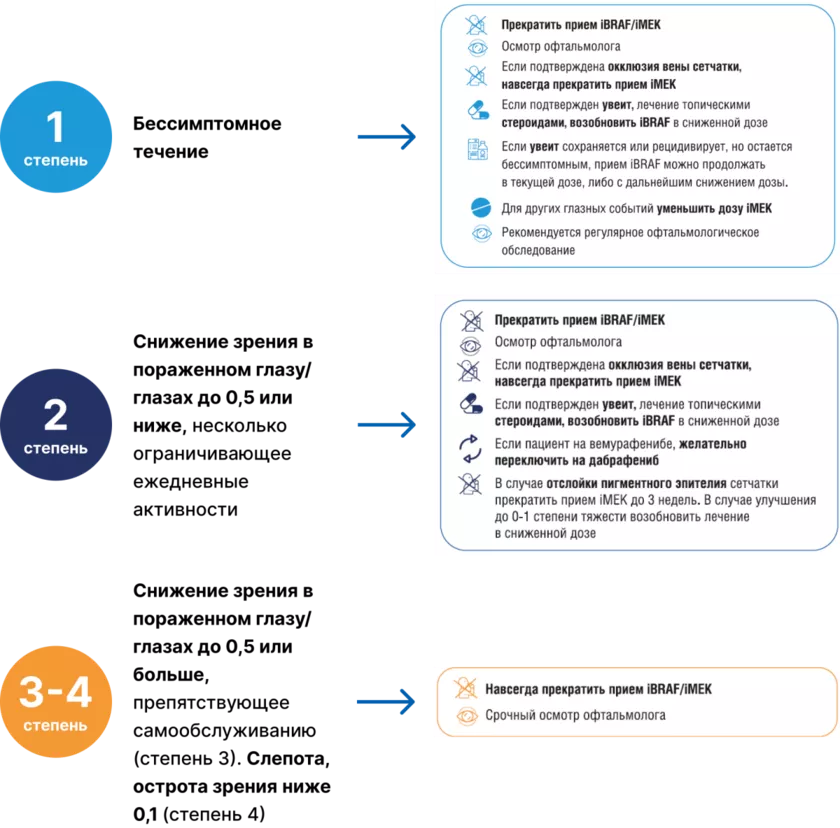
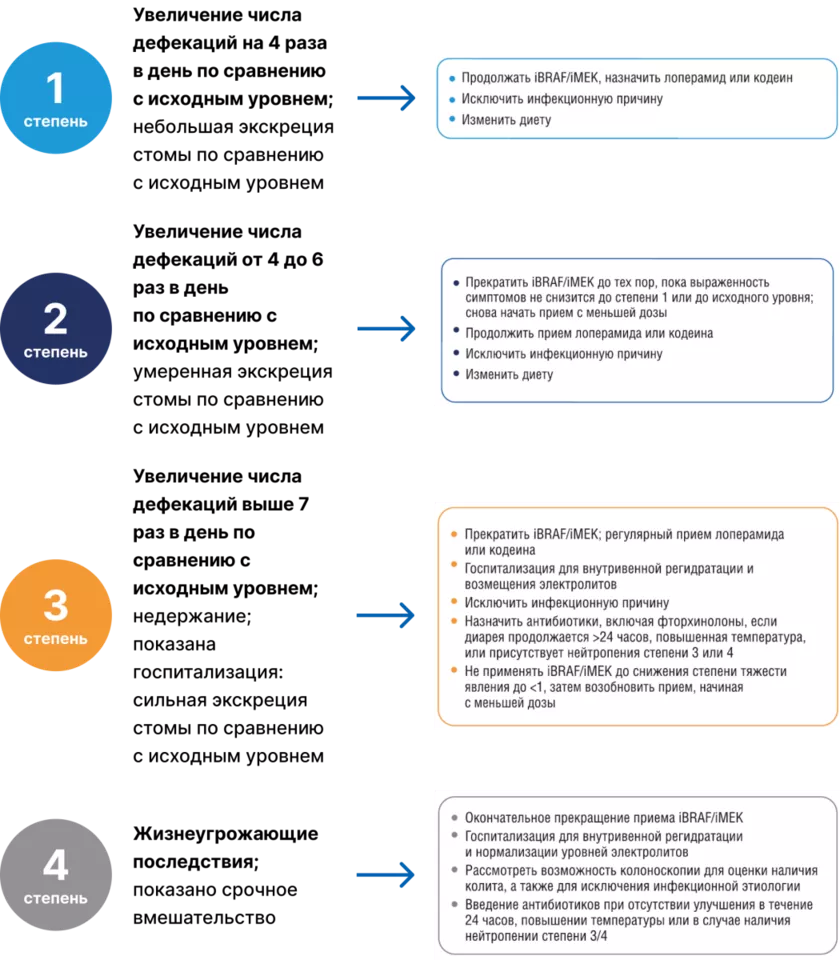
Диарея
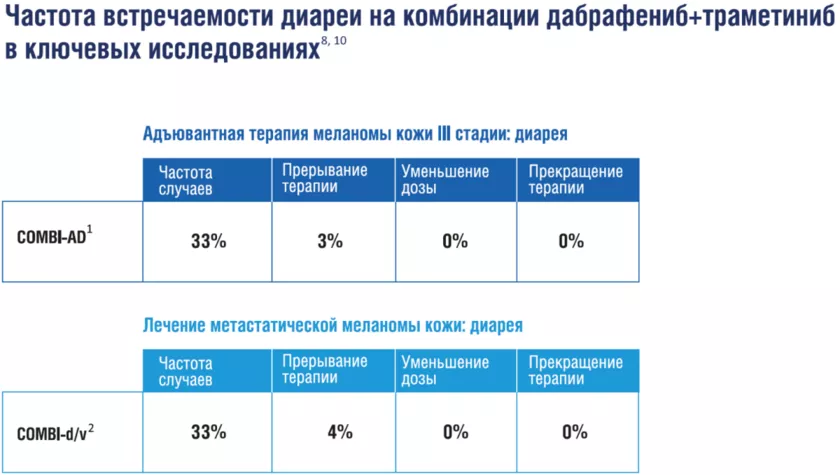
Алгоритм действий при офтальмологической токсичности [17]
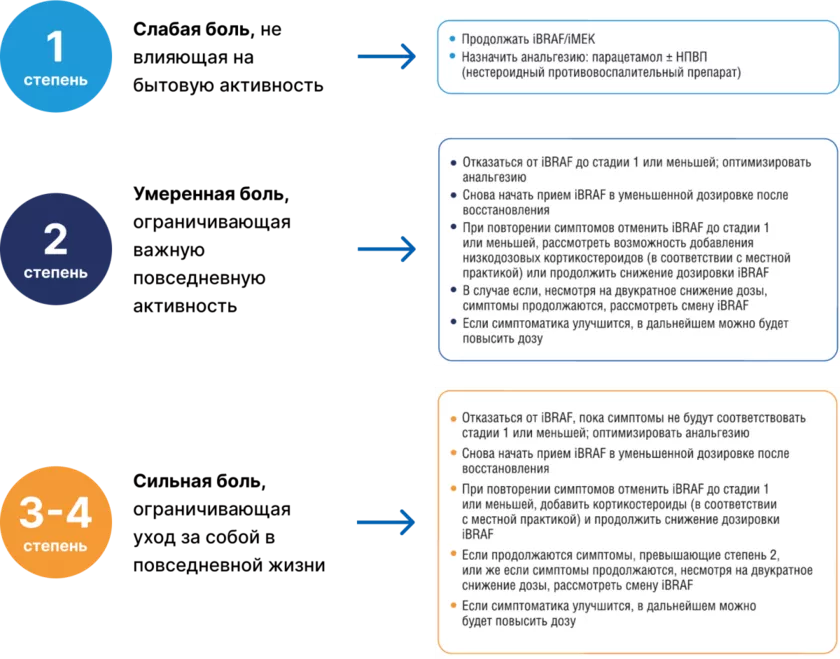
Артралгия

Алгоритм действий при артралгии [17]
НЯ со стороны сердечно-сосудистой системы

Алгоритм действий при удлинении интервала QT [17]
![Алгоритм действий при удлинении интервала QT [17] Алгоритм действий при удлинении интервала QT [17]](/ru-ru/sites/pro_novartis_com_ru/files/styles/twoup_layout_desktop_1080/public/2025-06/%D0%90%D0%BB%D0%B3%D0%BE%D1%80%D0%B8%D1%82%D0%BC%20%D0%B4%D0%B5%D0%B9%D1%81%D1%82%D0%B2%D0%B8%D0%B9%20%D0%BF%D1%80%D0%B8%20%D1%83%D0%B4%D0%BB%D0%B8%D0%BD%D0%B5%D0%BD%D0%B8%D0%B8%20.png.webp?itok=0Z8PBeP9)
Алгоритм действий при снижении ФВЛЖ [17]
![Алгоритм действий при снижении ФВЛЖ [17] Алгоритм действий при снижении ФВЛЖ [17]](/ru-ru/sites/pro_novartis_com_ru/files/styles/twoup_layout_desktop_1080/public/2025-06/%D0%90%D0%BB%D0%B3%D0%BE%D1%80%D0%B8%D1%82%D0%BC%20%D0%B4%D0%B5%D0%B9%D1%81%D1%82%D0%B2%D0%B8%D0%B9%20%D0%BF%D1%80%D0%B8%20%D1%81%D0%BD%D0%B8%D0%B6%D0%B5%D0%BD%D0%B8%D0%B8%20%D0%A4.png.webp?itok=KQzioFt8)
Алгоритм действий при развитии гипертензии [17]
![Алгоритм действий при развитии гипертензии [17] Алгоритм действий при развитии гипертензии [17]](/ru-ru/sites/pro_novartis_com_ru/files/styles/twoup_layout_desktop_1080/public/2025-06/%D0%90%D0%BB%D0%B3%D0%BE%D1%80%D0%B8%D1%82%D0%BC%20%D0%B4%D0%B5%D0%B9%D1%81%D1%82%D0%B2%D0%B8%D0%B9%20%D0%BF%D1%80%D0%B8%20%D1%80%D0%B0%D0%B7%D0%B2%D0%B8%D1%82%D0%B8%D0%B8%20%D0%B3.png.webp?itok=jwa6bSyy)
Гепатоксичность
Алгоритм действий при развитии гепатотоксичности [17]
![Алгоритм действий при развитии гепатотоксичности [17] Алгоритм действий при развитии гепатотоксичности [17]](/ru-ru/sites/pro_novartis_com_ru/files/styles/twoup_layout_desktop_1080/public/2025-06/%D0%90%D0%BB%D0%B3%D0%BE%D1%80%D0%B8%D1%82%D0%BC%20%D0%B4%D0%B5%D0%B9%D1%81%D1%82%D0%B2%D0%B8%D0%B9%20%D0%BF%D1%80%D0%B8%20%D1%80%D0%B0%D0%B7%D0%B2%D0%B8%D1%82%D0%B8%D0%B8%20%D0%B3%20%281%29.png.webp?itok=5Pd5PDdN)
Утомляемость
Алгоритм действий при развитии утомляемости [20]
![Алгоритм действий при развитии утомляемости [20] Алгоритм действий при развитии утомляемости [20]](/ru-ru/sites/pro_novartis_com_ru/files/styles/twoup_layout_desktop_1080/public/2025-06/%D0%90%D0%BB%D0%B3%D0%BE%D1%80%D0%B8%D1%82%D0%BC%20%D0%B4%D0%B5%D0%B9%D1%81%D1%82%D0%B2%D0%B8%D0%B9%20%D0%BF%D1%80%D0%B8%20%D1%80%D0%B0%D0%B7%D0%B2%D0%B8%D1%82%D0%B8%D0%B8%20%D1%83.png.webp?itok=DyR15tgb)
Как контролировать НЯ и снизить риск развития осложнений?

Список сокращений:
АЛТ — аланинаминотрансфераза; АСТ — аспартатаминотрансфераза; ЩФ — щелочная фосфатаза; МНО — международное нормализованное отношение; ОАК — общий анализ крови; НПВС — нестероидные противовоспалительные средства; АД — артериальное давление; ФВЛЖ — фракция выброса левого желудочка.
Список литературы
- Long G.V. et al. N Engl J Med. 2017;377(19):1813-1823.
- Atkinson V. et al. Eur J Cancer. 2022; 163:79-87.
- Dummer R. et al. N Engl J Med. 2020; 383(12):1139-1148.
- Atkinson A. et al. Adverse events over time in patients treated with adjuvant dabrafenib plus trametinib or placebo in the COMBI-AD trial. Presented at: ESMO 2018 Congress; October 19-23, 2018; Munich, Germany.
- Lee C.I. et al. Melanoma Res. 2014; 24(5):468-74.
- Menzies A.M. et al. Ann Oncol. 2015; 26(2):415-21.
- Welsh S.J., Corrie P.G. Ther Adv Med Oncol. 2015; 7(2):122-36.
- Hauschild A. et al. J Clin Oncol. 2018; 36(35):3441-3449.
- Pattipaka T. et al. Real-world characterization of pyrexia in melanoma patients treated with dabrafenib and trametinib. Presented at WCM/EADO 2021.
- Robert C. et al. N Engl J Med. 2019; 381(7):626-636.
- Dummer R. et al. J Clin Oncol. 2022; 40(13):1428-1438.
- Daud A. et al. J Hematol Oncol. 2017; 10(1):3.
- National Eye Institute. Eye Conditions and Diseases. https://www.nei.nih.gov/learn-about-eye-health/eye-conditions-and-diseases. Accessed 07.07.22.
- American Society of Retina Specialists. Branch retinal vein occlusion. https://www.asrs.org/patients/retinal-diseases/24/branch-retinal-vein-oc.... Accessed 07.07.22.
- Long G.V. et al. Ann Oncol. 2017; 28(7):1631-1639.
- Robert C. et al. Three-year estimate of overall survival in COMBI-v, a randomized phase 3 study evaluating first-line dabrafenib + trametinib in patients with unresectable or metastatic BRAF V600E/K–mutant cutaneous melanoma. Presented at ESMO 2016 Congress. Abstract LBA40.
- Welsh S.J., Corrie P.G. Management of BRAF and MEK inhibitor toxicities in patients with metastatic melanoma. Ther Adv Med Oncol. 2015; 7(2):122-36.
- Sinha R. et al. Cutaneous adverse events associated with vemurafenib in patients with metastatic melanoma: practical advice on diagnosis, prevention and management of the main treatment related skin toxicities. British Journal of Dermatology. 2012; 167(5):987-994.
- Adelmann C.H. et al. Comparative profiles of BRAF inhibitors: the paradox index as a predictor of clinical toxicity //Oncotarget. – 2016. – Т. 7. – №. 21. – С. 30453.
- Atkinson V. et al. Optimizing combination dabrafenib and trametinib therapy in BRAF mutation-positive advanced melanoma patients: Guidelines from Australian melanoma medical oncologists. Asia Pac J Clin Oncol. 2016; 12 (Suppl 7):5-12.
11235399/ONCO/DIG/07.24/0
