Presentaciones1
Viales de vidrio con 20 mg de basiliximab en forma de polvo liofilizado estéril para infusión o inyección intravenosa tras la reconstitución de la solución con 5 ml de agua para inyectables.
SIMULECT®
Basiliximab 20 mg

Beneficios
Facilita el esquema terapéutico con una administración de dos dosis estándar.1
Inmunosupresión más dirigida y con menor toxicidad.1
Alto perfil de seguridad, no requiere premedicación ni infusiones prolongadas.1
Es un medicamento selectivo para pacientes con bajo riesgo inmunológico que no requieren ser sometidos a una inmunosupresión alta.1
Indicaciones:1

Trasplante renal
Indicaciones completas aquí.
Profilaxis del rechazo agudo de órganos en trasplante renal de novo y debe utilizarse concomitantemente con inmunosupresión basada en ciclosporina para micro emulsión y corticosteroides
Dosificación




Modo de administración3,4
Una vez reconstituido, Simulect® puede administrarse en infusión intravenosa durante 20-30 minutos o en bolo intravenoso.
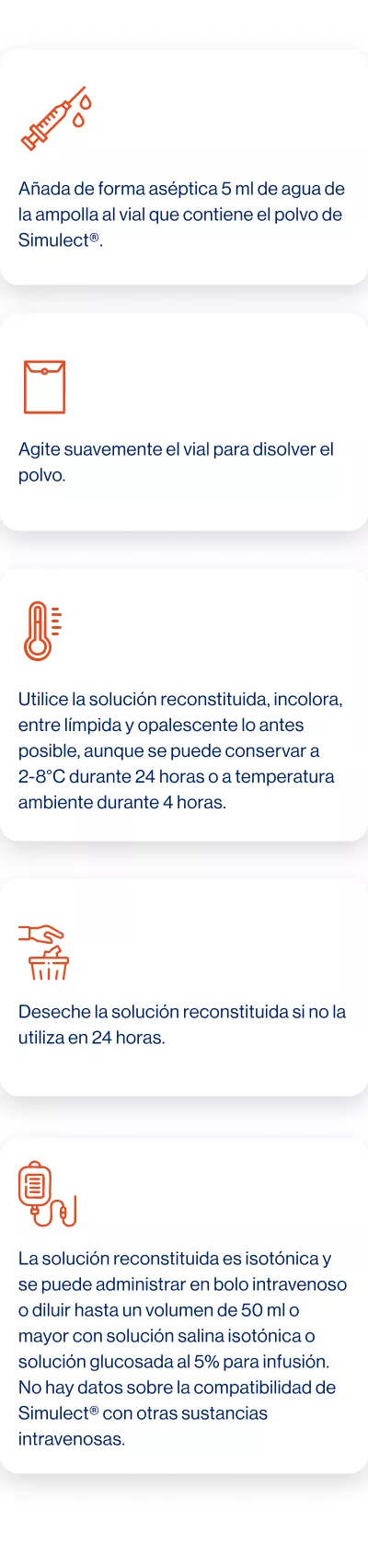
Instrucciones de uso y manipulación:

Referencias:
1. Simulect (basiliximab). Información del producto. Disponible desde: 13 de enero de 2014. Consultado: 13 de enero de 2014.
Novartis de Colombia S.A. Calle 93B No. 16-31 PBX: 654-4444. Bogotá D.C. Novartis de Colombia S.A. Novartis Pharma AG de Basilea, Suiza ® = Marca registrada. Material exclusivo para médicos. Para más información sobre el producto y sus indicaciones, comunicarse con el área de MIC (Medical Information & Communication) al siguiente correo electrónico: [email protected]. Más información en el Departamento Médico de Novartis S.A Colombia: 6544444. Si desea reportar un evento adverso ingrese al siguiente link: www.novartis.com/report. Este material es promocional en lenguaje, apariencia e intención. Este material no pretende sustituir o reemplazar una decisión clínica ni terapéutica. No se autoriza la grabación, toma de fotografías y distribución del material y tampoco difusión por medios no autorizados por Novartis Colombia. Content ID: FA-11504972. Fecha de aprobación: 28/11/2025. Fecha de caducidad: 28/11/2027.
Para más información consulte la información para la prescripción. Para acceder a la información para prescribir del producto escanee el código QR y asegúrese de seleccionar el producto o productos que contiene este material. Myfortic 360 mg Registro INVIMA 2022M-0002166-R2. Myfortic 180 mg Registro INVIMA 2022M-0002162-R2. En caso de no poder visualizar la información para prescribir del producto solicítela por medio del siguiente correo: informació[email protected]. Indicaciones: Myfortic está Indicado en asociación con ciclosporina y corticoides en la profilaxis del rechazo del trasplante, para pacientes receptores de alotrasplantes renales.



