Estudios MEASURE 1, 2 y 3: información completa y resultados
Un documento que abarca toda la información científica y análisis que se desprende del ensayo.
MEASURE 1 y 2
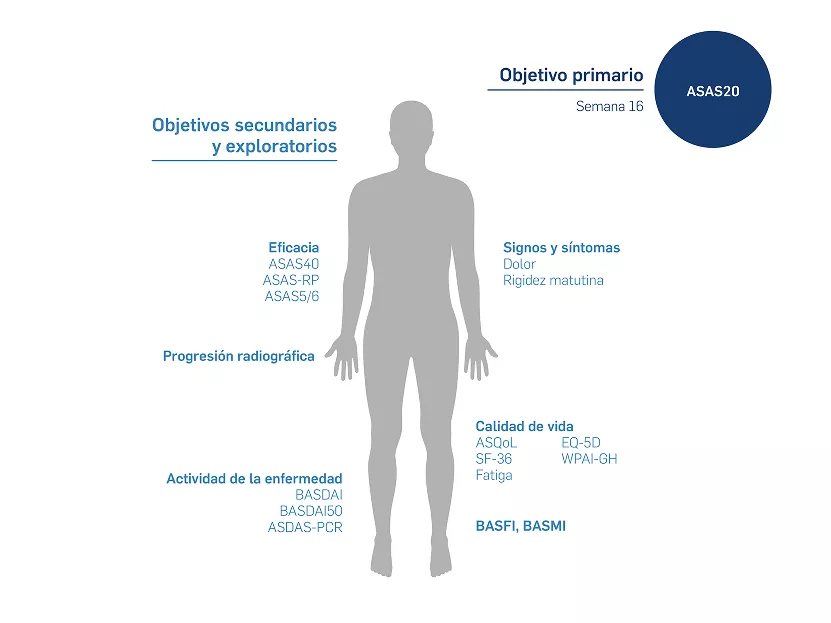
MEASURE 1 y 2, ensayos clínicos de fase III, multicéntricos, de doble ciego, aleatorizados y controlados con placebo, evaluaron la eficacia y seguridad de secukinumab pacientes con espondilitis anquilosante (EA).

En ambos estudios, la aleatorización se estratificó de acuerdo a la exposición previa a inhibidores de TNF (TNFi) en pacientes naïve y pacientes que habían tenic intolerancia o respuesta inadecuada a TNFi (TNF-IR).
El 84% de los pacientes completaron los 5 años de tratamiento con Secukinumab en el MEASURE1





MEASURE 3
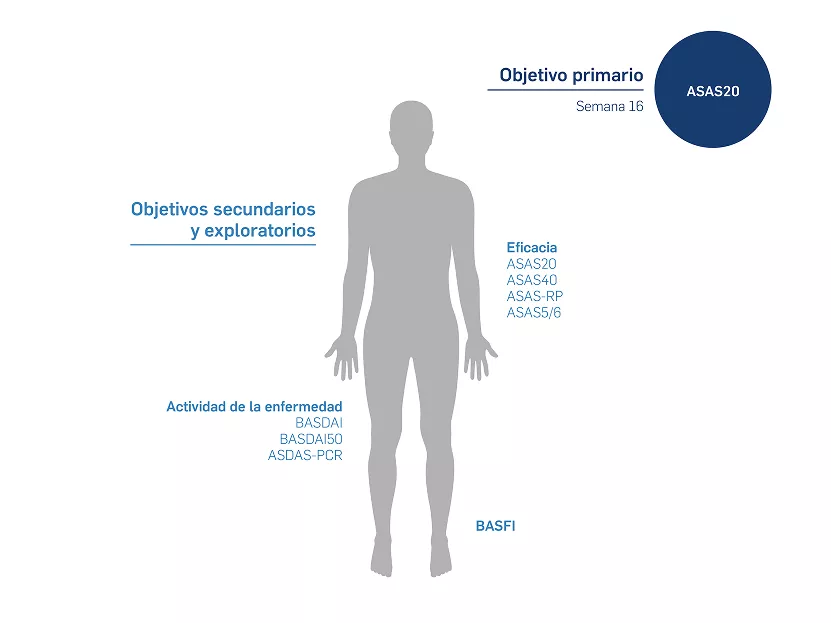
MEASURE 3 es un ensayo clinico de fase III, multicéntrico, de doble ciego, aleatorizado y controlado con placebo, de 3 años de duración, que evaluó la eficacia y seguridad de secukinumab en pacientes con espondilitis anquilosante (EA).

Un total de 226 pacientes (N=226) fueron incluidos en el estudio. La aleatorización se estratificó de acuerdo a la exposición previa a inhibidores de TNF (TNFi) e cientes naïve y pacientes que habían tenido intolerancia o respuesta inadecuada a TNFI (TNF-IR).
El 80% de los pacientes completaron los 3 años de tratamiento con Secukinumab


Conclusiones

A: aleatorización; ASAS: Assessment of SpondyloArthritis international Society: ASAS-RP: Assessment of SpondyloArthritis international Society - remisión parcial: ASDAS-PCR: Ankylosing Spondylitis Disease Activity Score-proteina C reactiva, ASQoL: Ankylosing Spondylitis Quality of Life, BASDAI: Bath Ankylosing Spondylitis Disease Activity Índice; BASFI: Índice funcional de espondilitis anquilosante de Bath: EQ-5D: Cuestionario de estado de salud de 5 dimensiones de calidad de vida en Europa; BASMI: Espondilitis Anquilosante en Baño Metrología: EA: Espondilitis Anquilosante; F: Última evaluación: FACIT-Fatigue: Functional Assessment of Chronic line Therapy-Fatigue Scale, I.v.: intravenoso, mSASSS: Stroke Ankylosing Spondylitis Spinal Score modificado; N: número de pacientes; s.c.: subcutáneo, SF-36: encuesta corta de 36 ítems: TNFI inhibidor del factor de necrosis tumoral: TNFI-RI: pacientes con intolerancia o respuesta inadecuada a TNFI: WPAI-GH: Work Productivity and Activity Impairment-General Health
Referencias
Baraliakos X. et al. RMD Open 2019;5:e001005
Baeten D. et al. N Engl J Med 2015;373:2534-48
Braun J. et al. Rheumatology 2019;58:859-868
Braun J. et al. Ann Rheum Dis 2017;76(6):1070-1077
Baraliakos X. [abstract]. Arthritis Rheumatol. 2017; 69 (suppl 10).
Deodhar A et al. Arthritis Rheumatol 2016;68:2901-2910
Baraliakos X. et al. Clin Exp rheumatol. 36(1):50-55
Deodhar A. et al. Clin Exp Rheumatol. 2019;37(2):260-269
Marzo-Ortega H et al. Lancet Rheumatol 2020;2:e339-46
Pavelka K. et al. ACR Open Rheumatol 2020;2(2):119-127.
Pavelka K. et al. Artritis Res Térmica. 2017;19(1):285.
