

Estudio PREVENT
“La espondiloartritis axial puede tener un impacto importante en la calidad de vida y la capacidad de un paciente para realizar actividades diarias. Los invitamos a conocer los resultados del estudio PREVENT, el cual demostró la eficacia y seguridad de Secukinumab en pacientes con espondiloartritis axial no radiográfica activa, mostrando un alivio temprano y sostenido de los signos y síntomas de la enfermedad"
Conocimientos clave

Antecedentes + Pacientes y diseño del estudio

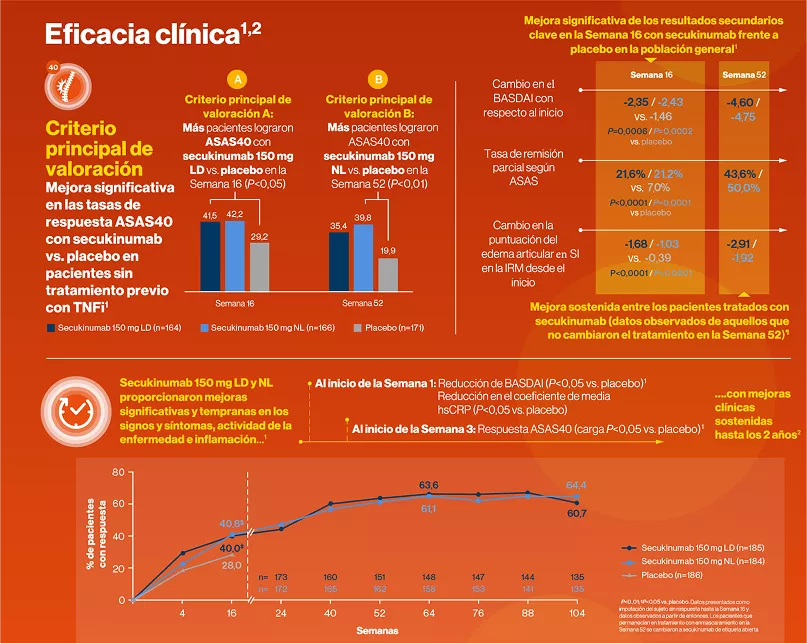
Eficacia clínica
Seguridad
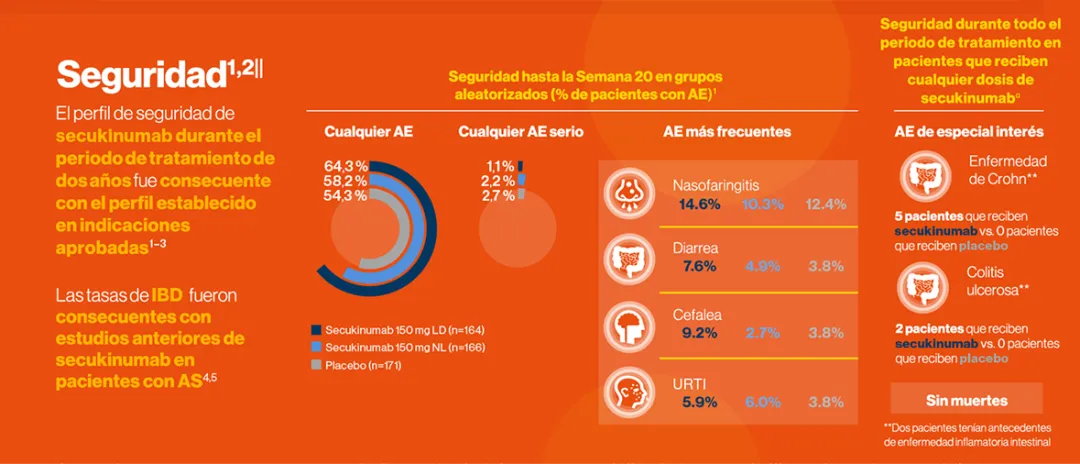
*Dolor de espalda inflamatorio durante ≥6 meses, inicio de la enfermedad a los <45 años de edad y sacroilitis en IRM con ≥1 característica de SpA o HLA–B27 positivo con ≥2 características deSpA.†IRM con inflamación de las articulaciones SI y/o PCR de alta sensibilidad superior al límite superior de normalidad.‡Los grupos de secukinumab150 mg LD y placebo recibieron dosis al inicio del estudio, Semanas 1, 2 y 3, y Q4W a partir de la Semana 4; el grupo de secukinumab 150 mg NL recibió dosis al inicio del estudio y Q4W a partir de entonces, con dosis de placebo administradas en las Semanas 1, 2 y 3 para mantener el enmascaramiento.§Para pacientes con respuesta inadecuada basada en el criterio clínico de actividad de la enfermedad (investigador y paciente).¶Se incluyeron datos de 78 pacientes en el grupo de LD de secukinumab 150 mg y84en el grupo de NL secukinumab 150 mg para cambios con respecto al valor inicial en la puntuación BASDAIy remisión parcial de ASAS, y de 81y 87 pacientes, respectivamente, para la puntuación de edema articular SI en la IRM.||Datos de seguridad presentados para el conjunto de análisis de seguridad, incluidos todos los pacientes que reciben ≥1dosis de tratamiento del estudio. α Incluye al menos 52 semanas para todos los pacientes y hasta 104 semanas para algunos; cualquier tratamiento consecukinumab incluye a los pacientes originalmente aleatorizados a secukinumab y a aquellos que cambiaron a secukinumab del placebo.βLas indicaciones de secukinumab (Cosentyx) en los Estados Unidos incluyen el tratamiento de adultos con AS activa y adultos con nr-axSpA activa con signosobjetivos de inflamación, y en Europaincluyen el tratamiento de: i) AS activo en adultos que han respondido inadecuadamente a la terapia convencional, y; ii)adultos con nr-axSpA activa con signos objetivos de inflamación, como lo indican laspruebas elevadas de PCRy/o IRM, que han respondido inadecuadamente a los fármacos antiinflamatorios no esteroideos. 6,7AE, evento adverso; AS, espondilitis anquilosante; ASAS,Evaluación de la Sociedad Internacional de Espondiloartritis; axSpA, espondiloartritis axial; BASDAI,Índice de Actividad de Bath para la Enfermedad Espondilitis Anquilosante; CRP, proteína Creactiva; hsCRP, CRP de alta sensibilidad; IBD, enfermedad inflamatoria intestinal; LD, dosis decarga; MRI, imágenes por resonancia magnética; NL, sin dosisde carga; nr-axSpA; espondiloartritis axialno radiográfica; Q4W, cada 4 semanas; s.c., subcutánea; SI, sacroilíaca; SpA,espondiloartritis; TNFi, inhibidor del factor denecrosis tumoral; URTI, infección del tracto respiratorio superior.
Referencias
Deodhar A, et al.ArthritisRheumatol. 2021;73:110–20;
Poddubnyy D, et al. EULAR 2021 (Abstract 143);
Deodhar A, et al.Arthritis Res Ther. 2019;21:111
Baeten D, et al.N Engl J Med. 2015;373:2534–48;
Baraliakos X, et al.RMD Open. 2019;5(2):e001005;
Cosentyx (secukinumab) Prescribing Information. Available at: https://www.accessdata.fda.gov/drugsatfda_docs/label/2020/125504s035lbl.pdf
Cosentyx (secukinumab) Summary of Product Characteristics. Available at: https://www.medicines.org.uk/emc/product/3669/smpc (Accessed April 2021);
Sieper J, Poddubnyy D.Lancet.2017;390:73–84;
Deodhar A, et al.AnnRheumDis.2016;75:791–4;
Lockwood MM, Gensler LS.BestPractResClinRheumatol.2017;31:816–29;
Malaviya AN, et al.IntJ Rheumatol.2017;2017:1824794;
Poddubnyy D, Rudwaleit M.Rheum Dis Clin North Am.2012;38:387–403.
