
NATALEE: РКИ III фазы для изучения эффективности и безопасности комбинации рибоциклиба с ингибитором ароматазы для адъювантной терапии HR+ HER2 − РМЖ II–III стадии
Дизайн исследования
NATALEE — открытое сравнительное исследование III фазы (n = 5101), проводимое с целью оценки эффективности и переносимости комбинации рибоциклиба (400 мг в сутки, 21 день прием, 7 дней перерыв; продолжительность приема 3 года) и нестероидного ингибитора ароматазы (ИА) (летрозола или анастрозола; продолжительность приема не менее 5 лет) по сравнению с монотерапией ИА.
В исследование включали следующих пациентов HR+ HER2− РМЖ II−III стадии:
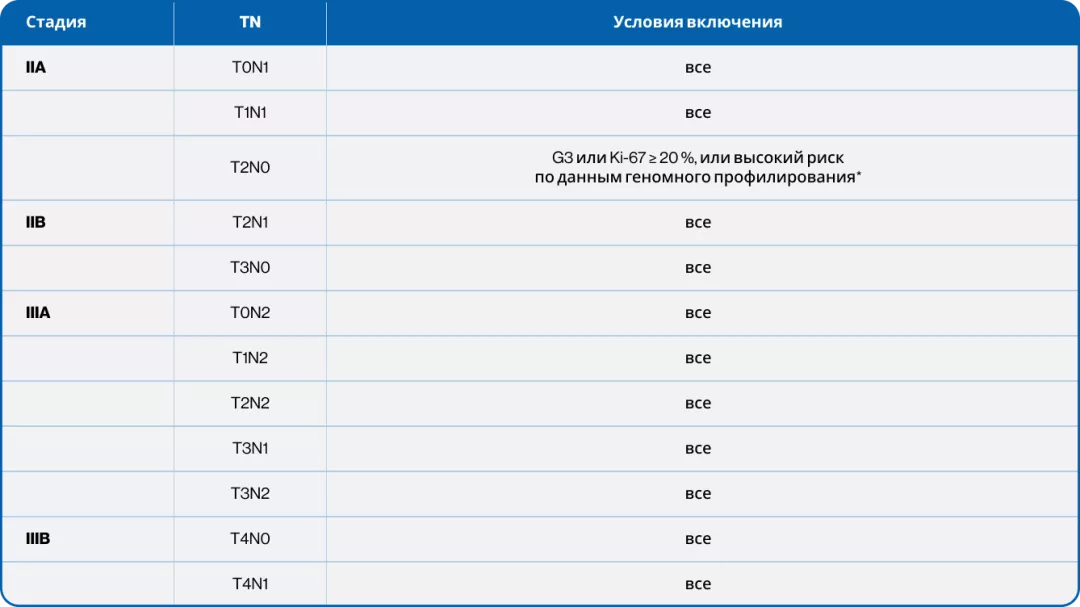
*OncotypeDx, MamaPrint, PAM50
По условиям протокола пациенты с II стадией составляли 40 % от всех пациентов. Дизайн исследования представлен на рис. 1.
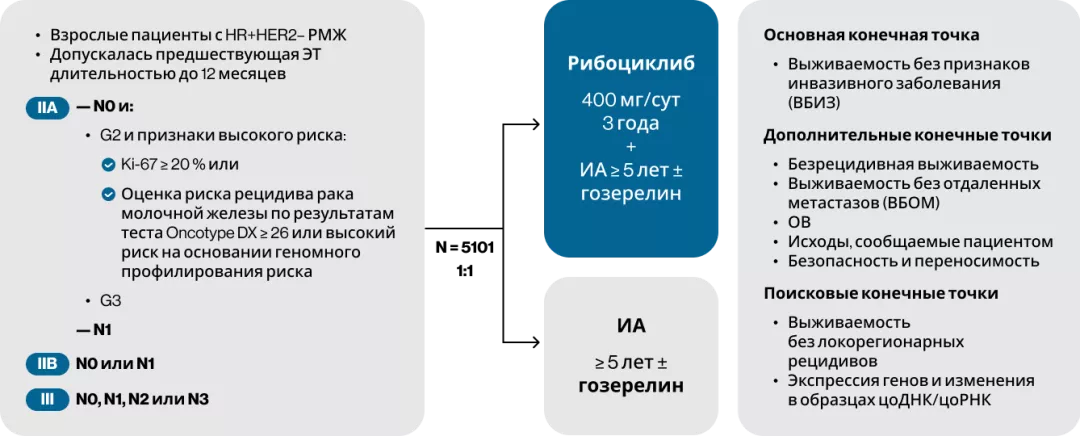
Рисунок 1. Дизайн исследования NATALEE
Исходные характеристики пациентов
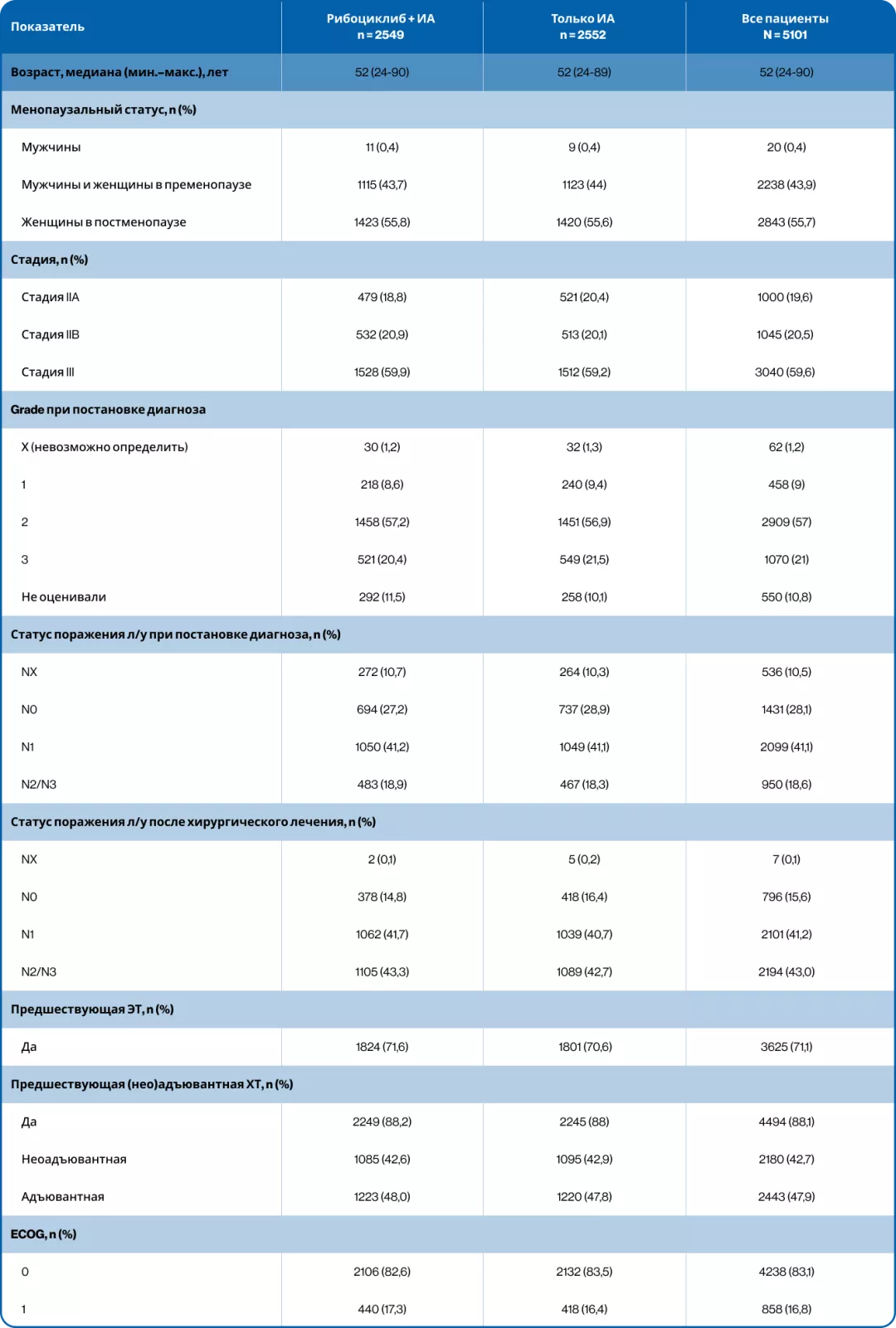
Набор в исследование проходил в период с января 2019 г. по апрель 2021 г. Ключевые исходные характеристики пациентов представлены в таблице 1.
Таблица 1. Исходные характеристики пациентов
Оценка эффективности
Первичная конечная точка - выживаемость без инвазивного заболевания (ВБИЗ)
В исследовании NATALEE рибоциклиб в комбинации с НСИА продемонстрировал статистически значимое преимущество в выживаемости без признаков инвазивного заболевания (ВБИЗ) по сравнению с терапией только НСИА в широкой популяции пациентов с HR+ HER2 − РМЖ (рис. 3).
На момент окончания сбора данных (25 мая 2025 г.) все пациенты, рандомизированные в группу рибоциклиба + ИА (n = 2549), прекратили получение рибоциклиба. Из них 62,8% (n = 1600) пациентов завершили 3-летний курс рибоциклиба, а 20,0% (n = 511) пациентов прекратили прием рибоциклиба досрочно из-за нежелательных явлений (НЯ). Медиана наблюдения для ВБИЗ составила 55,4 месяца (рисунок 2)8.
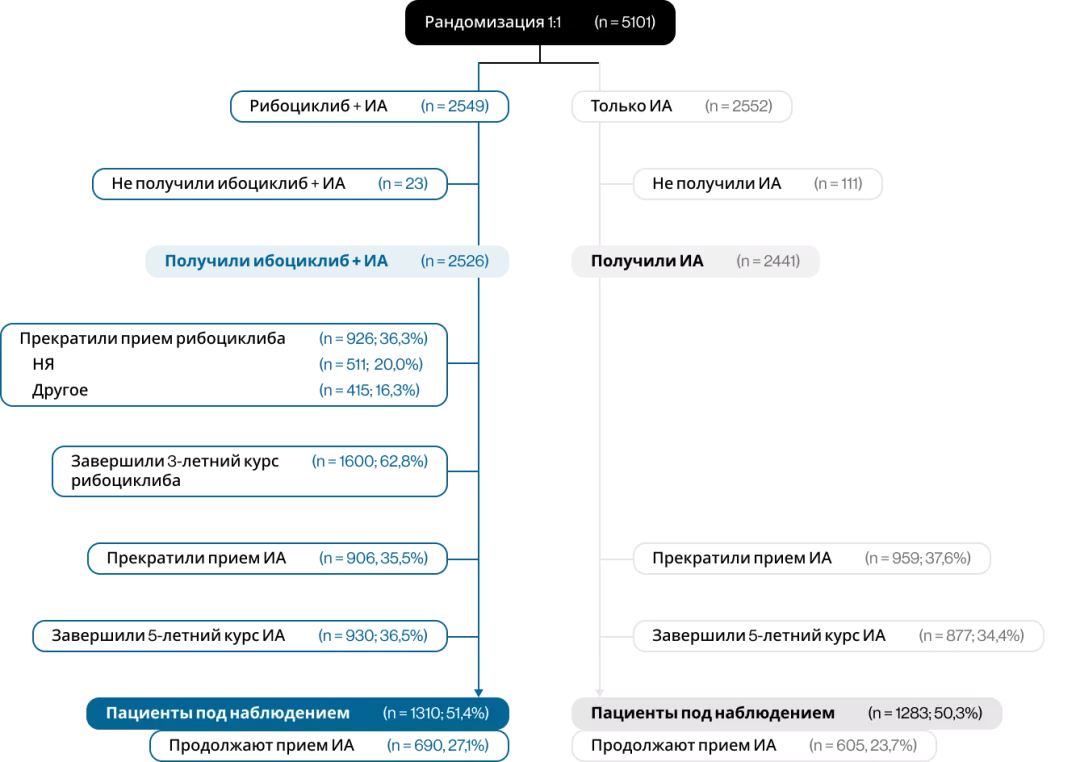
Рисунок 2. Распределение пациентов на момент проведения анализа (дата среза данных 25.05.2025)8
По результатам 5-летнего анализа ВБИЗ пациенты в группе рибоциклиба + ИА продолжили получать значительное преимущество по сравнению с пациентами в группе только ИА: абсолютное улучшение ВБИЗ через 3 года составляло 2,7%, а через 5 лет — уже 4,5%; снижение риска рецидива на 28,4% (рис. 3). Этот результат является статистически значимым: ОР 0,716 (95 % ДИ 0,618–0,829, p < 0,0001)4,8.
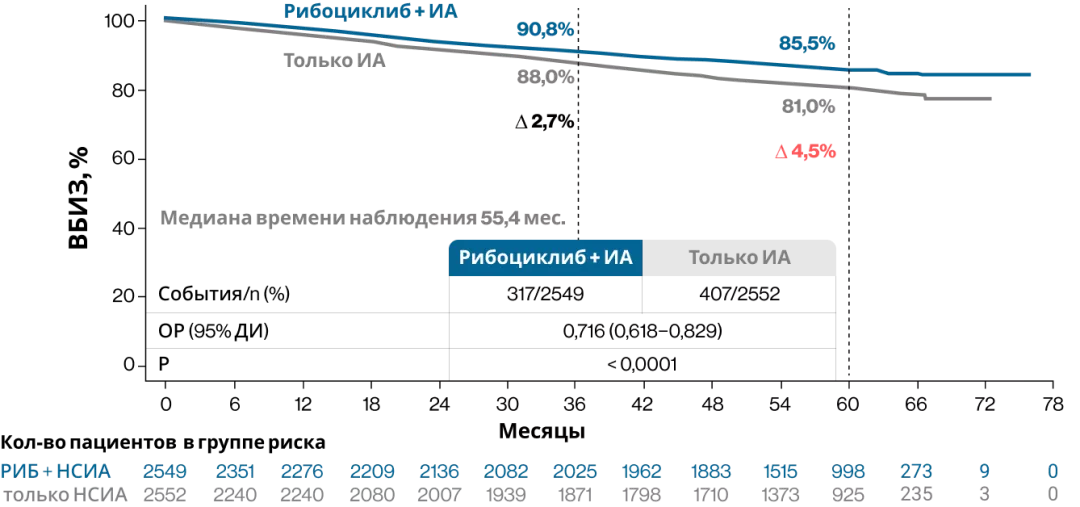
Рисунок 3. Выживаемость без признаков инвазивного заболевания в общей популяции пациентов в 5-летнем анализе исследования NATALEE
Улучшение ВБИЗ у пациентов, принимавших рибоциклиб, наблюдалось во всех исследованных подгруппах (рис. 4), в том числе с разным статусом поражения лимфоузлов (абсолютное улучшение ВБИЗ через 5 лет: в подгруппе N0–5,7%, в подгруппе N1-N3–4,4%) и разной стадией заболевания (стадия II−3,7%, стадия III−5,6%) (рис. 4–6)8.
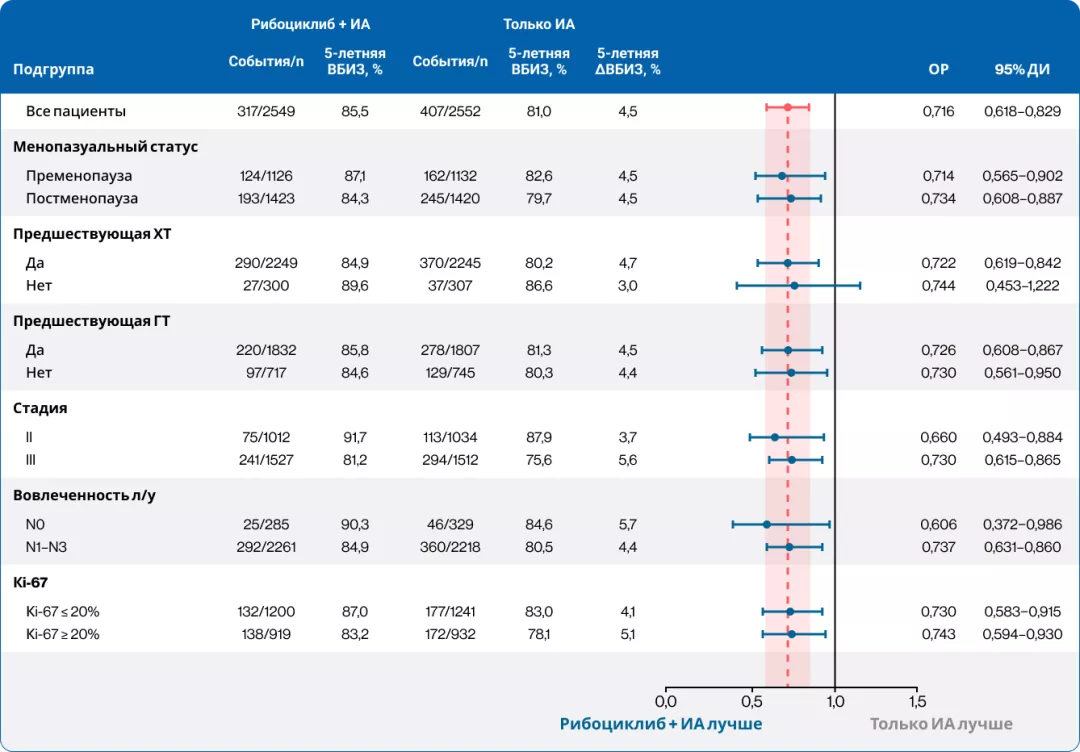
Рисунок 4. Подгрупповой анализ выживаемости без признаков инвазивного заболевания в 5-летнем анализе исследования NATALEE8
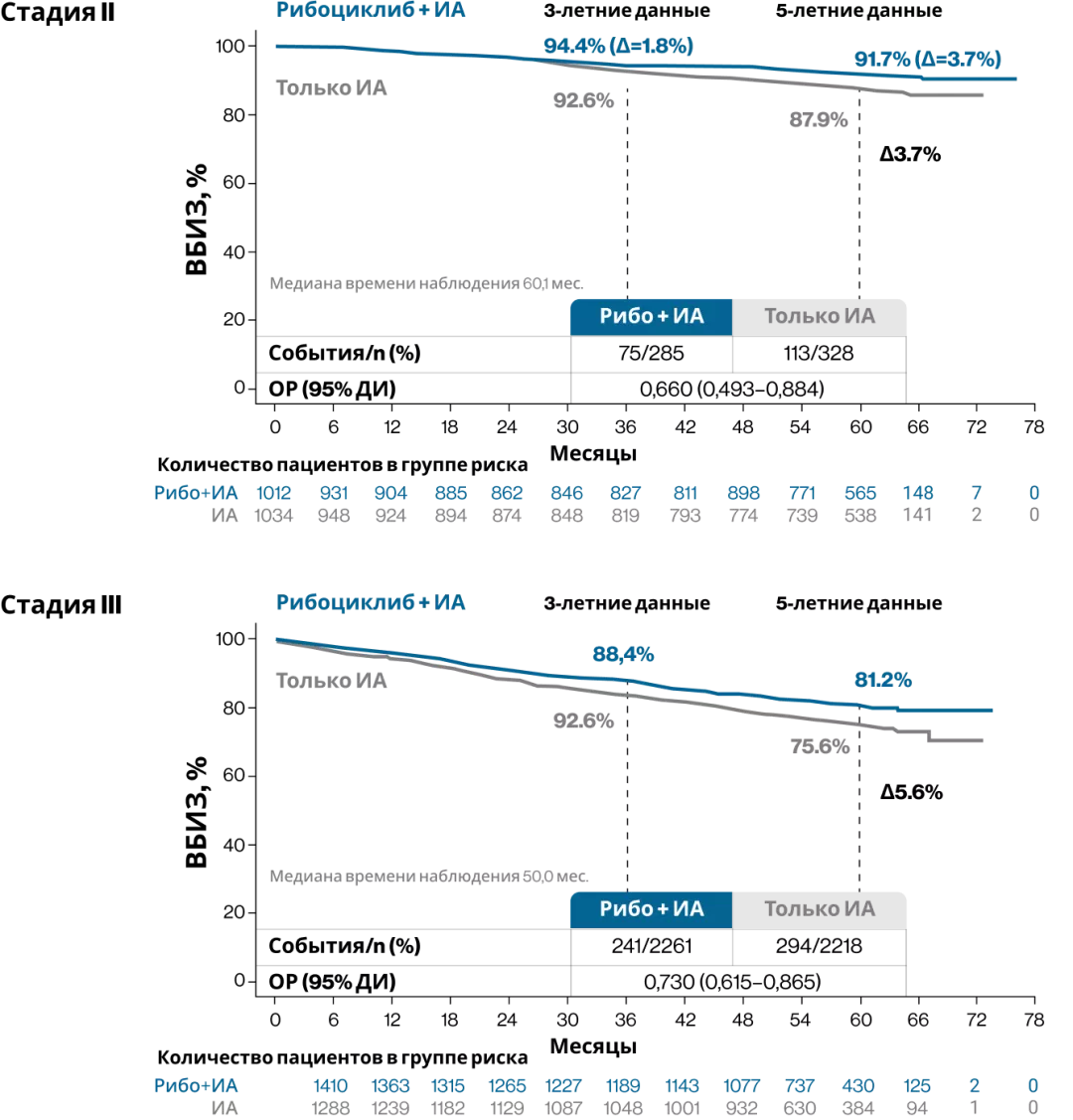
Рисунок 5. Выживаемость без признаков инвазивного заболевания у пациентов с II и III стадией8
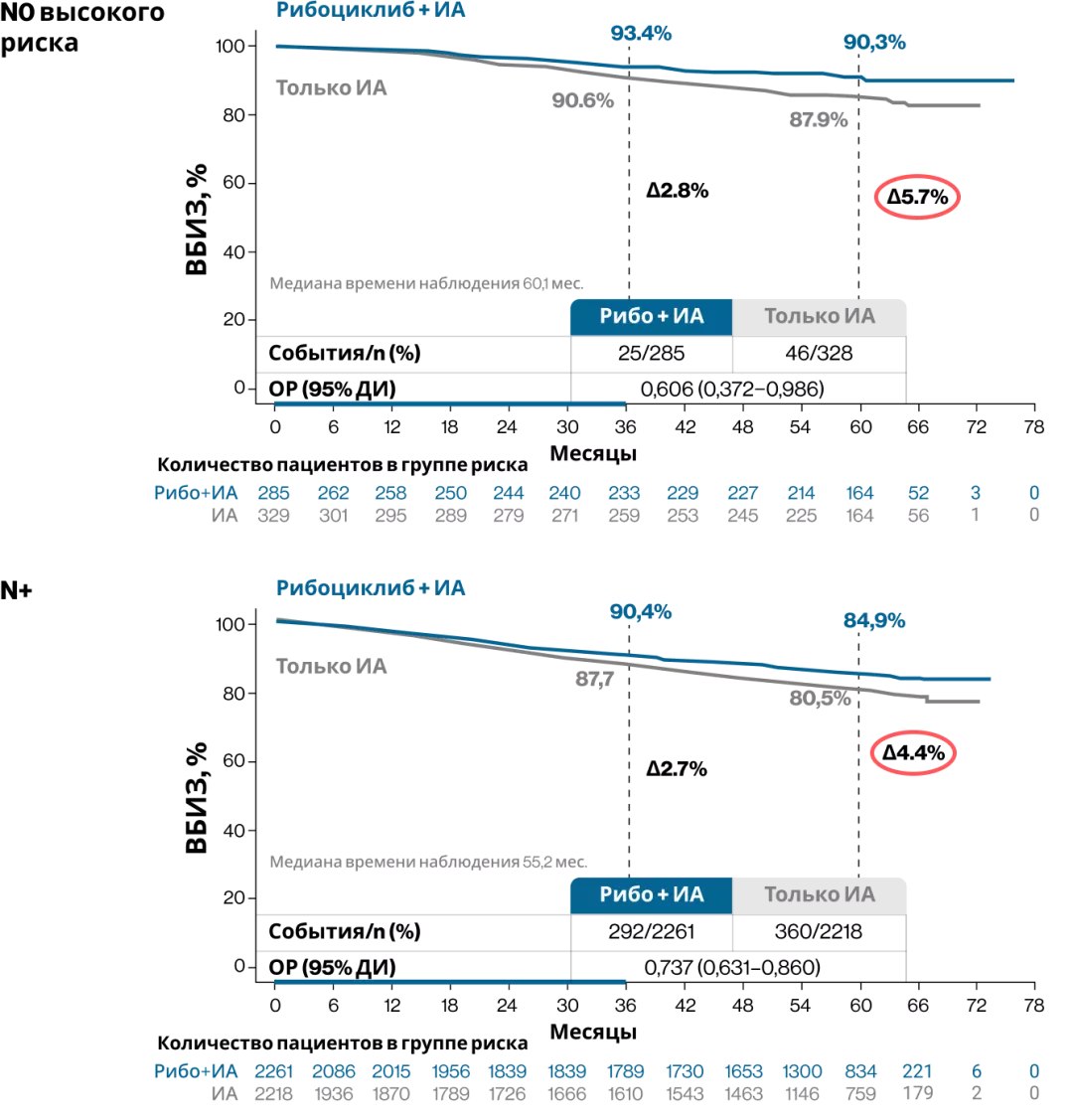
Рисунок 6. Выживаемость без признаков инвазивного заболевания при разном уровне поражения лимфоузлов8
Вторичные конечные точки − выживаемость без отдаленных метастазов (ВБОМ) и общая выживаемость (ОВ)
Кроме того, рибоциклиб + ИА по сравнению с монотерапией ИА продемонстрировал улучшение выживаемости без отдаленных метастазов (ВБОМ). В отношение общей выживаемости (ОВ) сохранялась тенденция к увеличению ОВ, однако данные еще не считаются зрелыми (рис. 7)8.
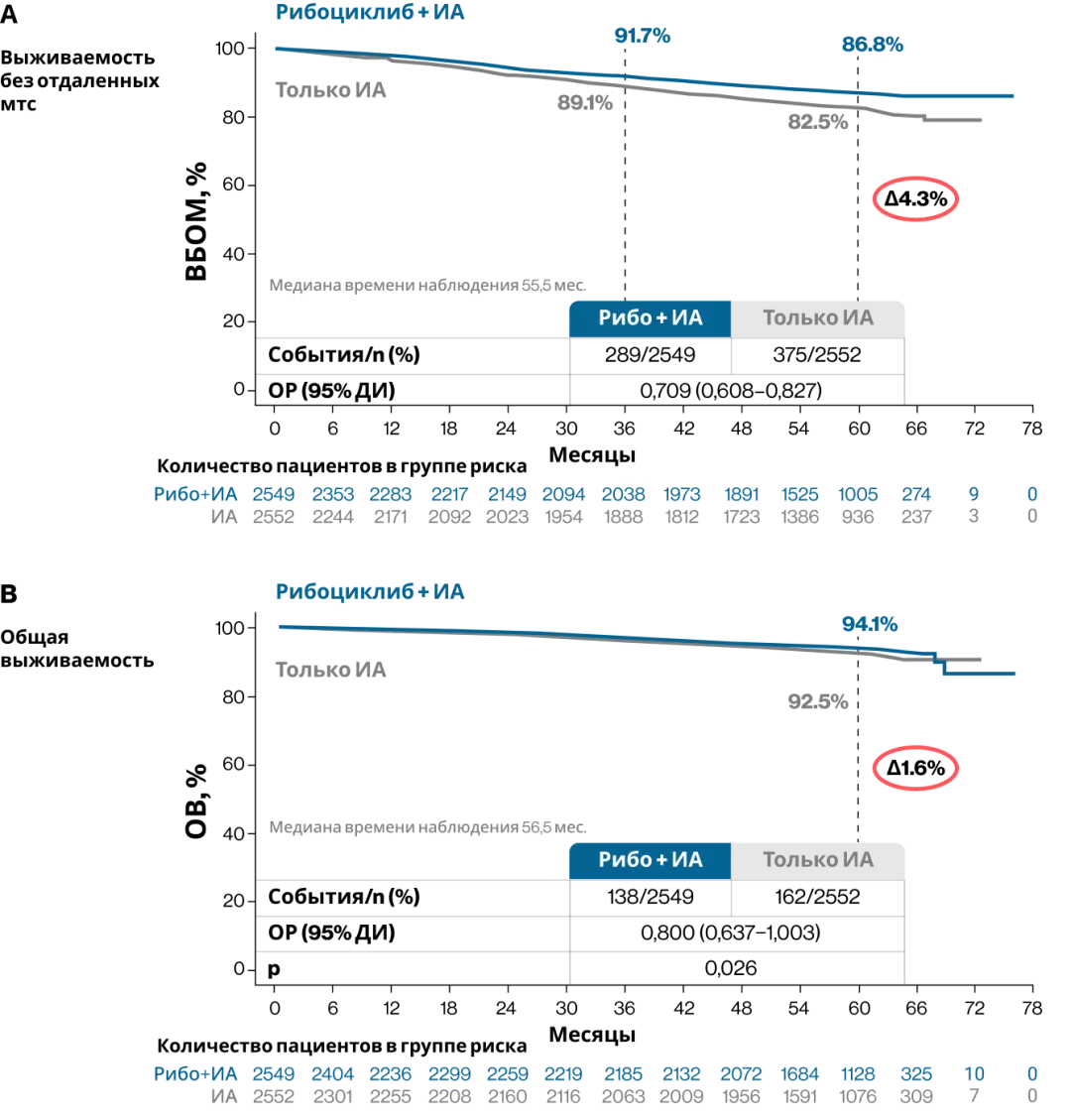
Рисунок 7. Выживаемость без отдаленных метастазов и общая выживаемость в общей популяции пациентов в 5-летнем анализе исследования NATALEE
Подгрупповой анализ ВБОМ продемонстрировал, что терапия рибоциклибом + ИА снижала риск отдаленных рецидивов у пациентов с HR+ HER2− ранним РМЖ, включая пациентов с заболеванием N0 высокого риска6. Преимущества в общей популяции и в ключевых клинически значимых подгруппах пациентов сохранялись после завершения запланированной 3-летней терапии рибоциклибом. Во всех подгруппах абсолютная польза от терапии рибоциклибом + ИА по сравнению с терапией только ИА увеличилась с течением времени (по мере накопления наблюдений с 3 до 4 лет)6.
В группе терапии рибоциклибом + ИА по сравнению с группой терапии только ИА через 4 года наблюдения улучшение ВБОМ происходило независимо от анатомической стадии РМЖ (табл. 2). С течением времени разница во ВБОМ между вариантами терапии увеличивалась6.
Таблица 2. Анализ ВБОМ в зависимости от стадии заболевания в исследовании NATALEE (4-летние данные)6
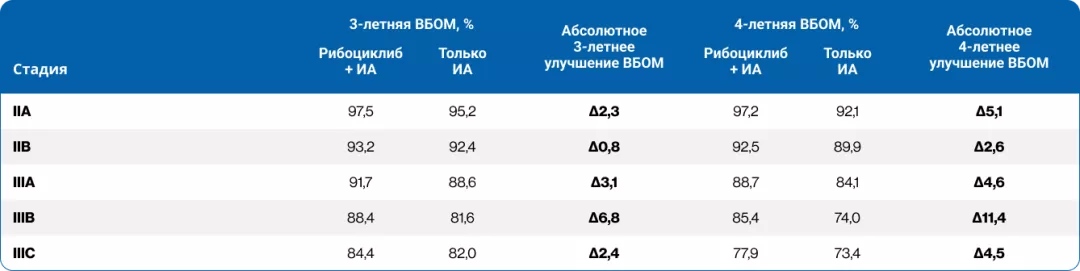
Таблица 3. Анализ ВБОМ в зависимости от статуса поражения лимфоузлов в исследовании NATALEE
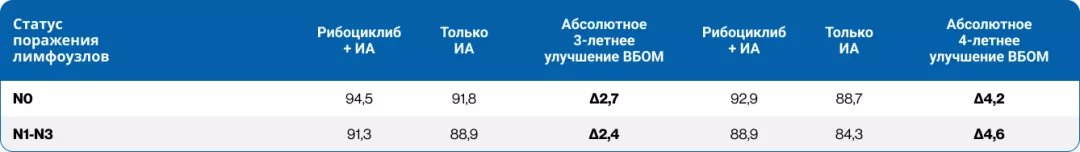
Терапия рибоциклибом + ИА привела к улучшению ВБОМ по сравнению с терапией только ИА у пациентов независимо от статуса менопаузы, Ki67, возраста и продолжительности предшествующей ЭТ с увеличением абсолютных 4-летних показателей по сравнению с 3-летними данными (табл. 4). Для всех подгрупп, за исключением пациентов, получавших предшествующую эндокринную терапию более 12 недель, улучшение ВБОМ было статистически достоверным6.
Таблица 4. Анализ ВБОМ в клинически значимых подгруппах пациентов в исследовании NATALEE (4-летние данные)6
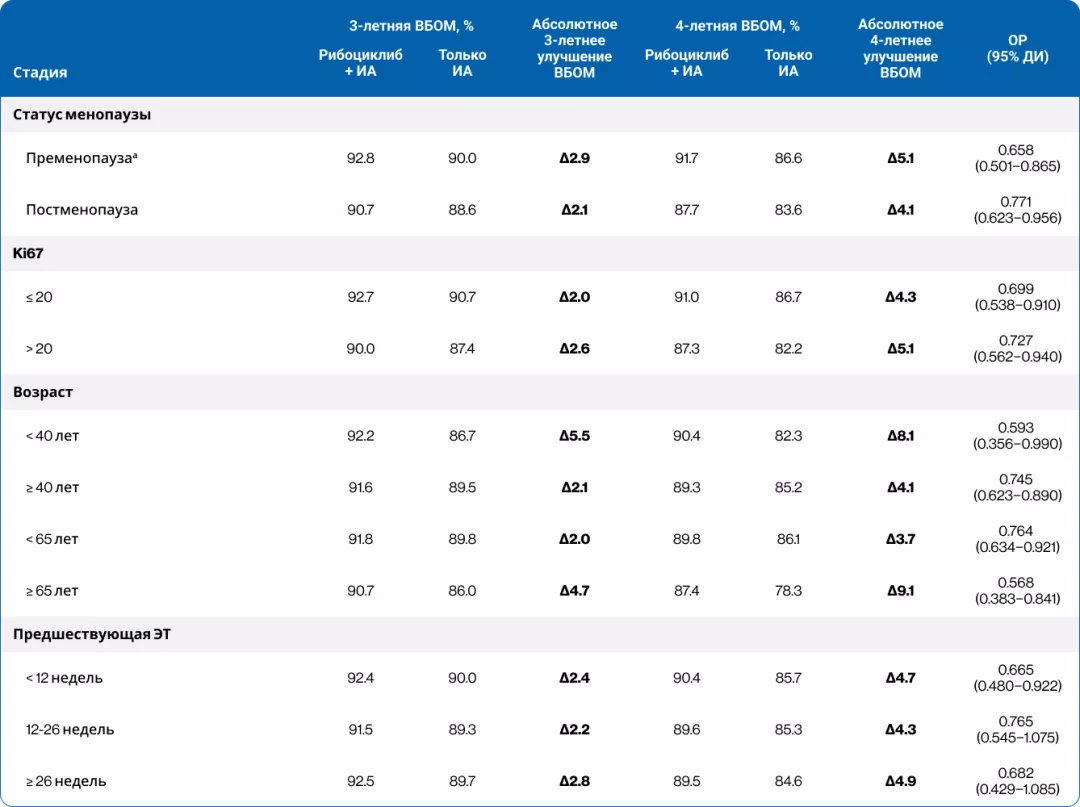
aВключая мужчин.
Переносимость терапии
Основные НЯ включали нейтропению и повышение печеночных ферментов (табл. 7)1,5,7.
Таблица 7. Переносимость терапии
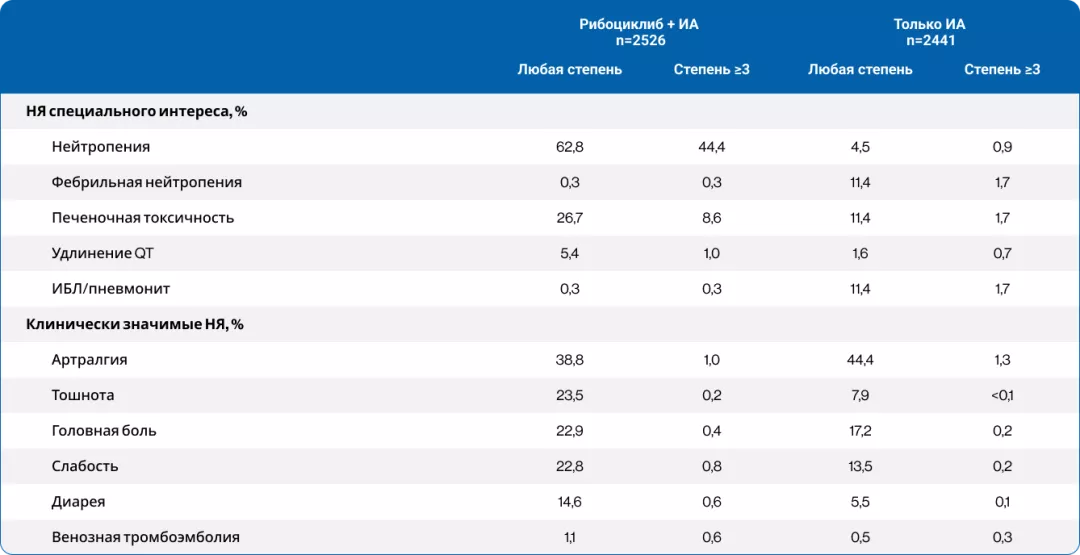
НЯ привели к снижению дозы рибоциклиба у 22,8% пациентов (14,6% - из-за нейтропении; 2,6% - из-за повышения АЛТ/АСТ). Медиана относительной интенсивности дозы рибоциклиба составила 94%.
Досрочное прекращение лечения рибоциклибом из-за НЯ потребовалось 20,0% пациентов (8,9% из-за повышения АЛТ/АСТ).
Анализ ВБИЗ показал, что снижение дозы рибоциклиба из-за НЯ не повлияло на эффективность лечения независимо от того, сколько времени прошло после начала лечения до редукции дозы (рис. 8)7.
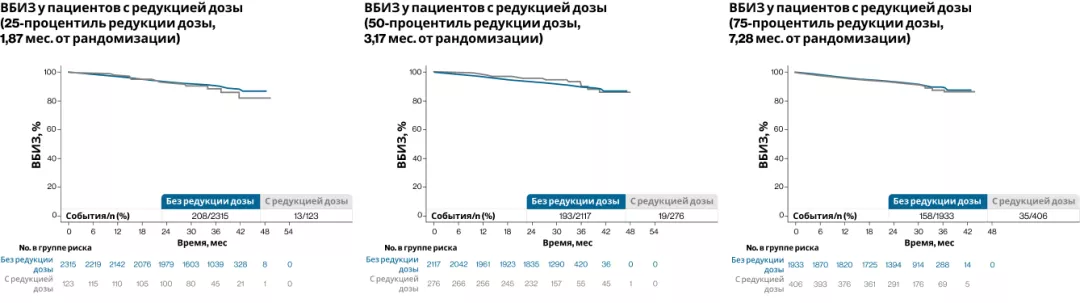
Рисунок 8. Выживаемость без признаков инвазивного заболевания (ВБИЗ) у пациентов, принимавших рибоциклиб в полной дозе (400 мг) и с редукцией дозы5
Список сокращений
ЭТ — эндокринная терапия;
л/у — лимфоузлы;
ХТ — химиотерапия;
ОВ — общая выживаемость;
ВБИЗ — выживаемость без признаков инвазивного заболевания;
ВБОМ — выживаемость без отдаленных метастазов;
ДИ — доверительный интервал;
ИА, НСИА — нестероидный ингибитор ароматазы;
ОР — отношение рисков.
*NATALEE — открытое сравнительное исследование III фазы (n = 5101), проводимое с целью оценки эффективности и переносимости комбинации рибоциклиба (400 мг в сутки, 21 день прием, 7 дней перерыв; продолжительность приема 3 года) и НСИА (летрозол или анастрозол; продолжительность приема не менее 5 лет) по сравнению с монотерапией НСИА. Первичная конечная точка достигнута: ВБИЗ через 3 года 90,7% vs 87,6% (ОР 0,749 (95%ДИ 0,628–0,892), p<0,0006).
Препарат рибоциклиб в комбинации с ингибитором ароматазы показан к применению для адъювантной терапии взрослых пациентов с положительным по гормональным рецепторам (HR+) и отрицательным по рецептору эпидермального фактора роста человека 2-го типа (HER2) ранним раком молочной железы III стадии или II стадии с высоким риском рецидива9.
Список литературы
- Slamon D., et al. Ribociclib plus Endocrine Therapy in Early Breast Cancer. N Eng J Med. 2024;390(12):1080-1091. https://doi.org/10.1056/NEJMoa2305488
- Slamon D., et al. Oral presentation at ASCO 2023. Oral LBA500.
- Hortobagyi G. et al. Ribociclib + Nonsteroidal Aromatase Inhibitor as Adjuvant Treatment in Patients With HR+/HER2− Early Breast Cancer: Final Invasive Disease–Free Survival Analysis From the NATALEE Trial. Presented at SABCS 2023. GS03-03.
- Fasching PA. Adjuvant Ribociclib (RIB) Plus Nonsteroidal Aromatase Inhibitor (NSAI) in Patients (Pts) With HR+/HER2− Early Breast Cancer (EBC): 4-Year Outcomes From the NATALEE Trial. LBA13. Proffered Paper presented at the European Society for Medical Oncology Congress, September 16, 2024. Barcelona, Spain.
- Fasching P. et al. JAMA Oncol. 2025:e253700. doi: 10.1001/jamaoncol.2025.3700.
- Hurvitz SA. Jarzab M. Mateu MM. et al. Distant disease-free survival (DDFS) across key subgroups from the phase 3 NATALEE trial of ribociclib (RIB) plus a nonsteroidal aromatase inhibitor (NSAI) in patients with HR+/HER2− early breast cancer (EBC). SABCS 2024. December 12, 2024. Poster presentation #P4-09-22.
- Burris H.A., et al. Safety and impact of dose reductions on efficacy in the randomised MONALEESA-2, -3 and -7 trials in hormone receptor-positive, HER2-negative advanced breast cancer. Br J Cancer. 2021;125:679-686. https://doi.org/10.1038/s41416-021-01415-9
- Crown J. et al. ESMO Open. 2025. https://doi.org/10.1016/j.esmoop.2025.105858
- Общая характеристика лекарственного препарата Рисарг® (рибоциклиб) таблетки, покрытые пленочной оболочкой, 200 мг (РУ ЛП-№(003228)-(РГ-RU)) от 06.10.2025 доступна по ссылке https://www.novartis.com/ru-ru/about/products.
1546463/RIB/web/11.25/0