Хронические нежелательные явления при адъювантной иммуноонкологической терапии меланомы кожи

Применение новых методов адъювантной терапии — иммуноонкологической терапии (ИТ) и таргетной терапии (ТТ) — значительно увеличило безрецидивную выживаемость пациентов после радикального удаления меланомы кожи. Однако спустя непродолжительное время после внедрения ИТ в клиническую практику в литературе стали появляться сообщения о случаях перехода иммуноопосредованных нежелательных явлений (иоНЯ), развившихся на фоне лечения ИТ, в хроническую форму1, 2. Тщательный анализ этого явления требует времени, но в последние несколько лет сообщения появляются все чаще.
Частота развития хронических иоНЯ
По данным более ранних исследований частота развития хронических иоНЯ у пациентов на фоне ИТ достигает 41–43%, в том числе 12% случаев — иоНЯ 3–4 степени тяжести1, 2. Большинство хронических иоНЯ связаны с1, 2:
- нарушениями работы эндокринной системы (чаще всего гипотиреоз и гипертиреоз);
- заболеваниями опорно-двигательного аппарата (чаще всего артрит и артралгия);
- кожными заболеваниями (дерматит).
Новые данные по развитию хронических иоНЯ
В 2023 году были опубликованы результаты нового ретроспективного мультицентрового когортного исследования американских и австралийских ученых, посвященного оценке рисков развития хронических иоНЯ у пациентов, получавших ИТ после резекции меланомы кожи III–IV стадии. Авторы проанализировали частоту развития иоНЯ у 318 пациентов (табл. 1, 2). Срок наблюдения составил не менее 1,5 лет (медиана 2,9 года) после прекращения адъювантной терапии3.

Таблица 1. Характеристика острых, хронических и стойких иоНЯ, развившихся на фоне ИТ3.
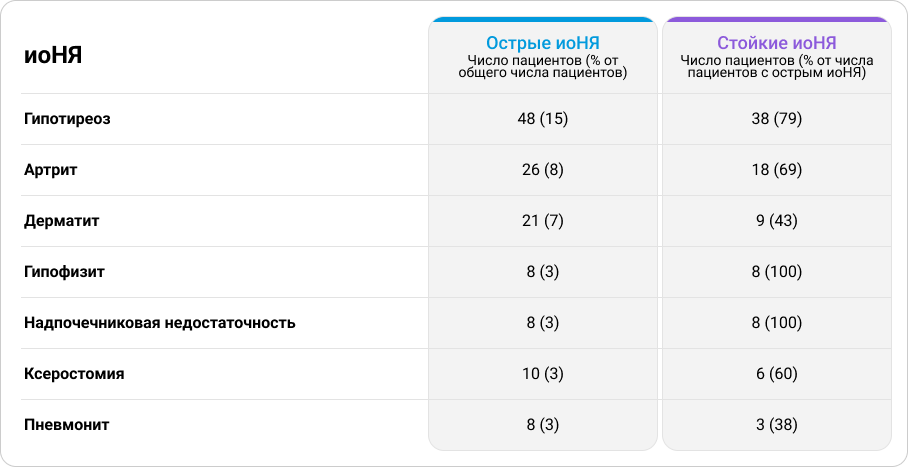
Таблица 2. Частота перехода иоНЯ на фоне ИТ в стойкую форму3.
Приведенные авторами исследования цифры заставляют задуматься о цене, которую пациент может заплатить за возможную пользу от адъювантной ИТ3.
Можно ли сказать, что риск развития хронических иоНЯ оправдан более высокой эффективностью ИТ по сравнению с ТТ? Непрямое сравнение регистрационных исследований показывает, что по эффективности выигрывает адъювантная ТТ. Так, например, 1-летняя безрецидивная выживаемость (БРВ) в группе дабрафениб + траметиниб в исследовании COMBI-AD составила 88%4 против 75% у пациентов, принимающих пембролизумаб, в исследовании Keynote-0545. Через 5 лет преимущество ТТ сохранилось: 5-летнее снижение риска рецидива 49%4 против 39%6. Кроме того, преимущество адъювантной ТТ перед ИТ анти-PD-1 препаратами подтверждается и данными реальной клинической практики7, 8.
Учитывая, что адъювантная ТТ превосходит ИТ по параметрам эффективности и при этом не вызывает хронических иоНЯ, выбор метода адъювантной терапии после резекции BRAF+ меланомы становится более очевидным1—5.
Выводы
У 46% пациентов, получавших адъювантную ИТ после удаления меланомы, развились хронические иоНЯ3.
- 50% хронических иоНЯ были ≥ 2 степени тяжести3.
- Большая часть (68%) хронических иоНЯ сопровождалась клинически выраженными симптомами3.
Частота развития стойких иоНЯ, сохранившихся к концу срока наблюдения за пациентами, составила 30%, из них 44% — с клинически выраженными симптомами3.
Список сокращений
БРВ — безрецидивная выживаемость;
ИТ — иммуноонкологическая терапия;
иоНЯ — иммуноопосредованные нежелательные явления;
НЯ — нежелательные явления;
ТТ — таргетная терапия.
Список литературы
- Patrinely J. R. et al. Chronic immune-related adverse events following adjuvant anti–PD-1 therapy for high-risk resected melanoma // JAMA oncology. – 2021. – Т. 7. – №. 5. – С. 744-748.
- Tong J. et al. Long-term toxicities of immune checkpoint inhibitor (ICI) in melanoma patients // Current Oncology. – 2022. – Т. 29. – №. 10. – С. 7953-7963.
- Goodman R.S. et al. Extended Follow-Up of Chronic Immune-Related Adverse Events Following Adjuvant Anti–PD-1 Therapy for High-Risk Resected Melanoma // JAMA Network Open. – 2023. – Т. 6. – №. 8. – С. e2327145-e2327145.
- Dummer R. et al. Five-year analysis of adjuvant dabrafenib plus trametinib in stage III melanoma // New England Journal of Medicine. – 2020. – Т. 383. – №. 12. – С. 1139-1148.
- Eggermont A. M. M. et al. Longer follow-up confirms recurrence-free survival benefit of adjuvant pembrolizumab in high-risk stage III melanoma: updated results from the EORTC 1325-MG/KEYNOTE-054 trial // Journal of clinical oncology. – 2020. – Т. 38. – №. 33. – С. 3925.
- Eggermont A. M. M. et al. Five-year analysis of adjuvant pembrolizumab or placebo in stage III melanoma // NEJM evidence. – 2022. – Т. 1. – №. 11. – С. EVIDoa2200214.
- Haist M. et al. Treatment management for BRAF-mutant melanoma patients with tumor recurrence on adjuvant therapy: a multicenter study from the prospective skin cancer registry ADOREG // Journal for Immunotherapy of Cancer. – 2023. – Т. 11. – №. 9.
- Bai X. et al. Dabrafenib plus trametinib versus anti-PD-1 monotherapy as adjuvant therapy in BRAF V600-mutant stage III melanoma after definitive surgery: a multicenter, retrospective cohort study // EClinicalMedicine. – 2023. – Т. 65.
11244866/ONCO/DIG/08.24/0