
Клиническое исследование Секукинумаб
Эффективность и безопасность секукинумаба при энтезит-ассоциированном артрите и ювенильном псориатическом артрите: результаты рандомизированного двойного слепого плацебо-контролируемого исследования 3 фазы с отменой лечения (junipera).
Эффективность
Несмотря на то, что современные стратегии лечения ЭАА и юПсА способствуют облегчению боли, их эффективность часто ограничена1, что требует начала более интенсивной терапии, включая введение биологических БМАРП, из которых лишь некоторые одобрены для лечения ЭАА и юПсА2,3
Цель
Цель данного исследования III фазы: продемонстрировать эффективности и безопасности секукинумаба у пациентов с активной формой ЭАА и юПсА с недостаточным ответом на стандартную терапию.
Дизайн исследования
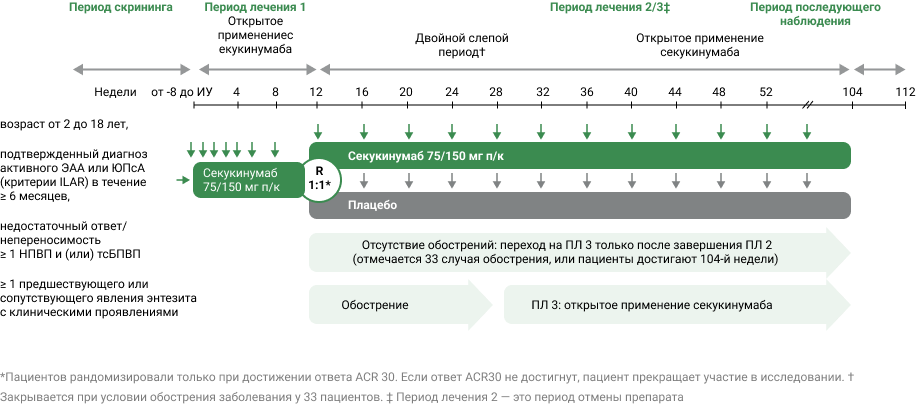
Основные критерии включения и исключения
Критерии включения
- Возраст пациентов от ≥ 2 до < 18 лет на момент скрининга
- Пациенты с активной формой заболевания, классифицированным в соответствии с критериями классификации ILAR ЮИА как ЭАА или юПсА
- Пациенты, ранее не получавшие биологические БМАРП, и с недостаточным ответом на терапию ≥ 1 тсБМАРП или НПВП
- Длительность заболевания ≥ 6 месяцев
Критерии исключения
- Активное неконтролируемое ВЗК или неконтролируемый увеит
- Пациенты, соответствующие любой категории ЮИА согласно классификации ILAR, кроме ЭАА или юПсА
- Текущие воспалительные заболевания в фазе обострения, отличные от юПсА/ЭАА, которые могут повлиять на пользу терапии секукинумабом
- Гиперчувствительность к любому из исследуемых препаратов или его компонентам в анамнезе или к препаратам аналогичных химических классов
Оценки
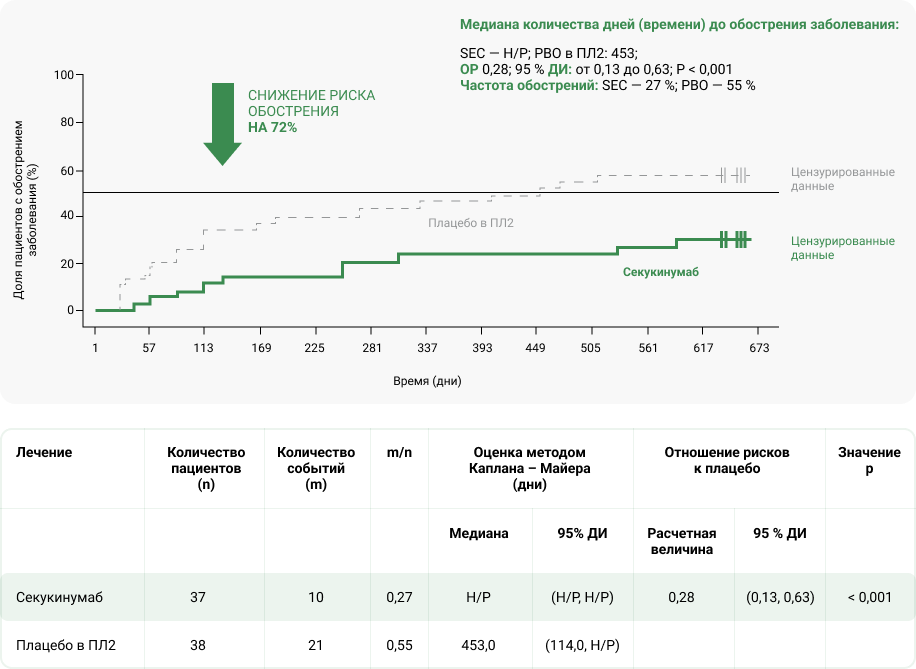
Время до обострения ЮИА в общей популяции
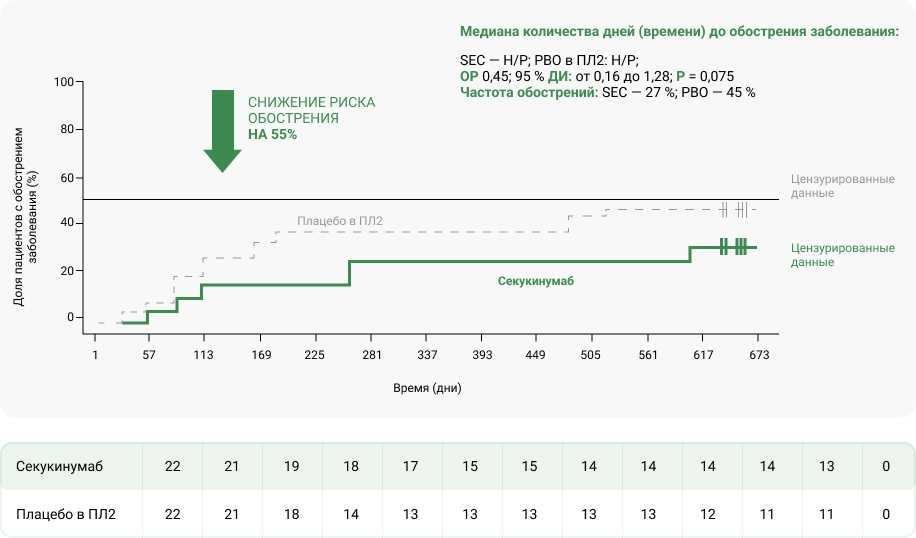
Время до развития обострения ЮИА в подкатегории ЭАА
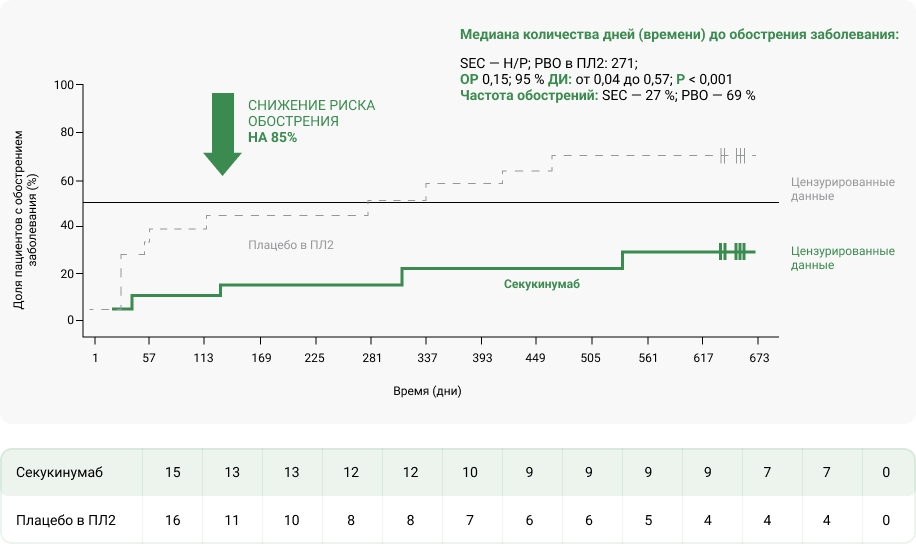
Время до развития обострения ЮИА в подкатегории юПсА
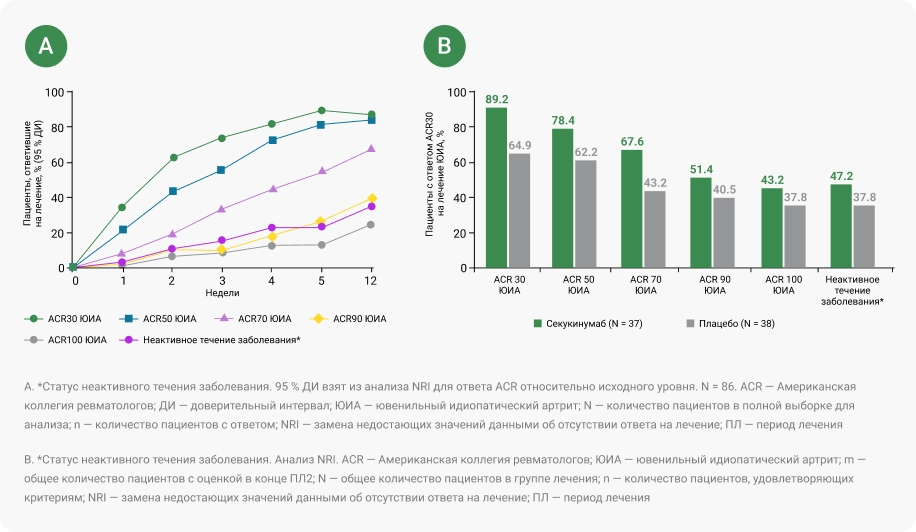
Ответы ЮИА ARC в открытом периоде лечения 1 (ПЛ1, A) и в конце периода лечения 2 (ПЛ2, B)
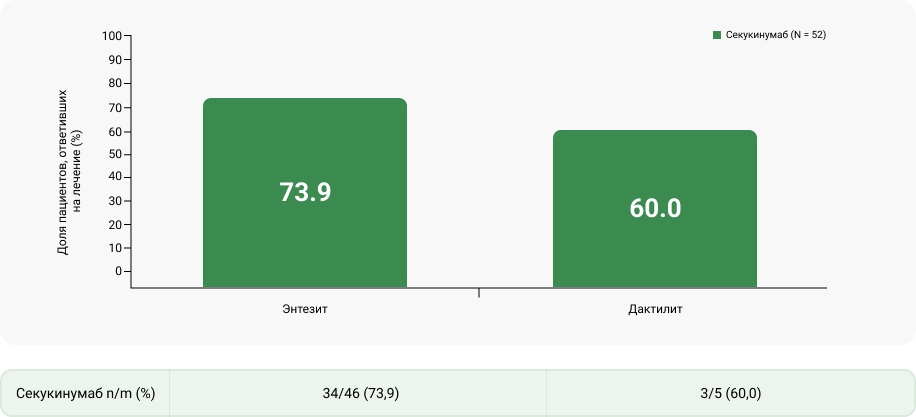
Пациенты с ЭЭА с полностью разрешившимся энтезитом и дактилитом на 12-й неделе — период лечения 1
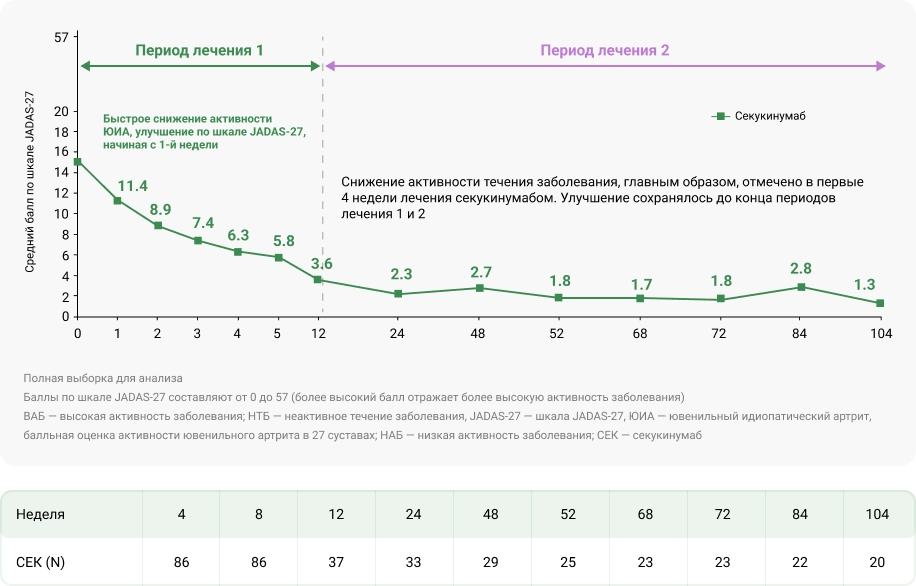
Средние значения по шкале JADAS-27 для пациентов, проходивших лечение секукинумабом во время периодов лечения 1 и 2
Обзор данных по безопасности за весь период лечения (выборка для оценки безопасности)
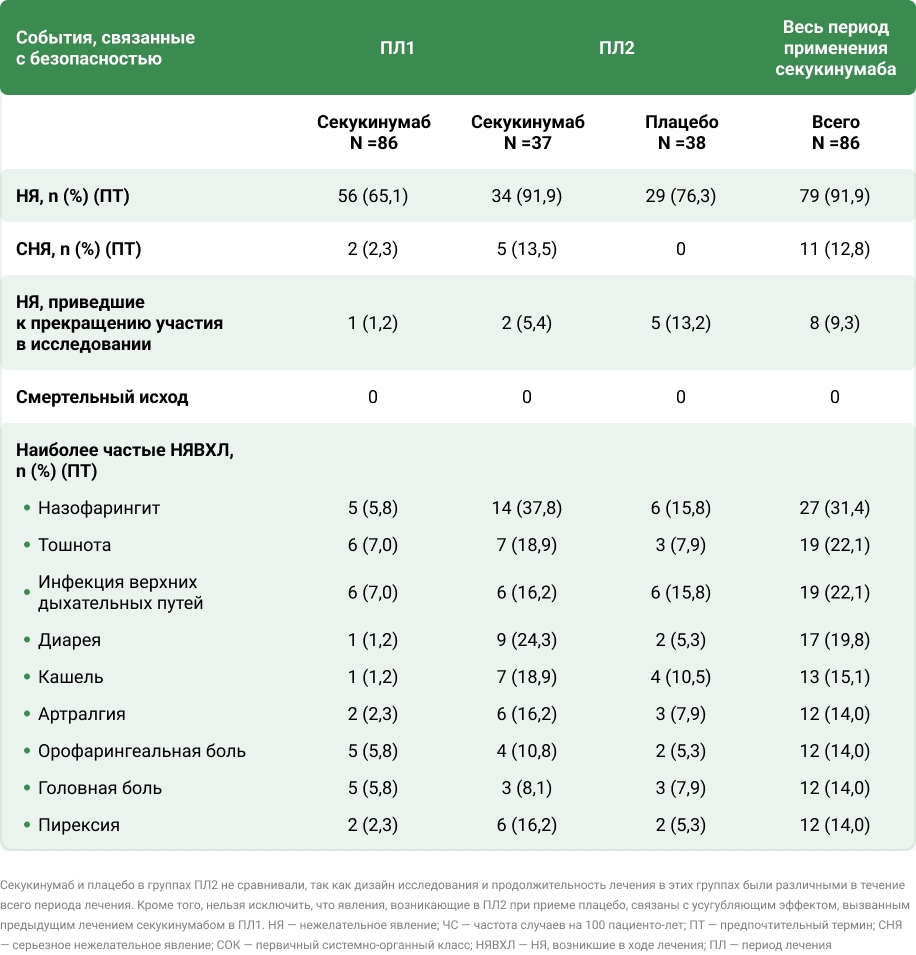
НЯ, возникшие в ходе лечения, за весь период лечения (выборка для анализа безопасности)

Список сокращений
Биологические БМАРП — биологические болезнь-модифицирующие антиревматические препараты;
ЭАА — энтезит-ассоциированный артрит;
юПсА — ювенильный псориатический артрит;
ИУ — исходный уровень;
тсБМАРП — традиционный синтетический болезнь-модифицирующий антиревматический препарат;
ILAR — Международная лига по борьбе с ревматизмом (от англ. International League Against Rheumatism);
НПВП — нестероидный противовоспалительный препарат;
R — рандомизированный;
П/К — подкожно;
ПЛ — период лечения;
ГИБП — генно-инженерные биологические препараты;
ВЗК — воспалительное заболевание кишечника;
ЮИА — ювенильный идиопатический артрит;
ACR — Американская коллегия ревматологов;
НЯ — нежелательные явления;
СР — стадия ремиссии;
JADAS — шкала активности ювенильного артрита;
MedDRA — медицинский словарь для регуляторной деятельности;
PRCSG — Группа по совместным исследованиям в области детской ревматологии;
PRINTO — Международная организация исследований в области детской ревматологии;
СНЯ — серьезные НЯ;
НЯВХЛ — НЯ, возникшие в ходе лечения;
ДИ — доверительный интервал;
ОР — отношение рисков;
Н/Р — не рассчитано;
PBO — плацебо;
SEC — секукинумаб;
ВАБ — высокая активность заболевания;
НТБ — неактивное течение заболевания;
ЧС — частота случаев на 100 пациенто-лет;
ПТ — предпочтительный термин;
СНЯ — серьезное нежелательное явление;
СОК — первичный системно-органный класс;
N — общее количество пациентов;
M — число пациентов, у которых было отмечено какое-либо значение.
Список литературы
- Guzman J. и соавт. J Rheumatol. 2017; 44: 230–40;
- Ravelli A. и соавт. Ann Rheum Dis. 2018; 77: 819–28;
- Burgos-Vargas R. и соавт. Arthritis Care Res (Hoboken). 2015; 67: 1503–12;
- Brunner HI, et al. Ann Rheum Dis. 2022 Aug 12:annrheumdis-2022-222849. doi: 10.1136/ard-2022-222849;
- Wallace CA. и соавт. Arthritis Care Res (Hoboken). 2011; 63: 929–36.
11308511/SEC/DIG/11.24/0