Терапия ОМЛ ингибиторами протеинкиназ
Поскольку наличие мутаций FLT3 ассоциировано с неблагоприятным прогнозом ОМЛ, последние российские и международные клинические рекомендации предписывают добавление к схеме лечения препаратов FLT3-ингибиторов (ингибиторов протеинкиназы)1–5.
Мидостаурин — первый препарат группы ингибиторов протеинкиназ, одобренный для лечения впервые выявленного положительного по FLT3-мутации ОМЛ. Мидостаурин назначается в сочетании со стандартной индукционной и консолидирующей химиотерапией, далее может быть назначена поддерживающая монотерапия мидостаурином.
В исследовании приняли участие 3277 пациентов в возрасте от 18 до 59 лет, у которых был впервые выявлен положительный по FLT3-мутации ОМЛ. Пациенты были рандомизированы для получения стандартной химиотерапии (индукционная терапия даунорубицином и цитарабином и консолидирующая терапия высокими дозами цитарабина) в сочетании с мидостаурином либо с плацебо. При достижении ремиссии после консолидирующей терапии пациенты на этапе поддерживающей терапии получали мидостаурин или плацебо. Рандомизация была стратифицирована в соответствии с подтипом мутации FLT3: TKD, ITD с высоким и ITD с низким аллельным соотношением.
Основные результаты исследования6:
- Значимое увеличение медианы общей выживаемости: 25,6 месяца в группе плацебо и 74,7 месяца в группе мидостаурина (рис. 1).
- Снижение риска летального исхода на 22% при добавлении мидостаурина к схеме лечения по сравнению с проведением только стандартной химиотерапии (отношение рисков 0,78, 95% ДИ 0,63–0,96, p = 0,009).
- У пациентов, получавших мидостаурин, наблюдалось значимое удлинение медиан бессобытийной и безрецидивной выживаемости по сравнению со стандартной химиотерапией в сочетании с плацебо.
- Мидостаурин демонстрирует благоприятный профиль безопасности: частота возникновения нежелательных явлений в группе мидостаурина сопоставима с таковой в группе плацебо.
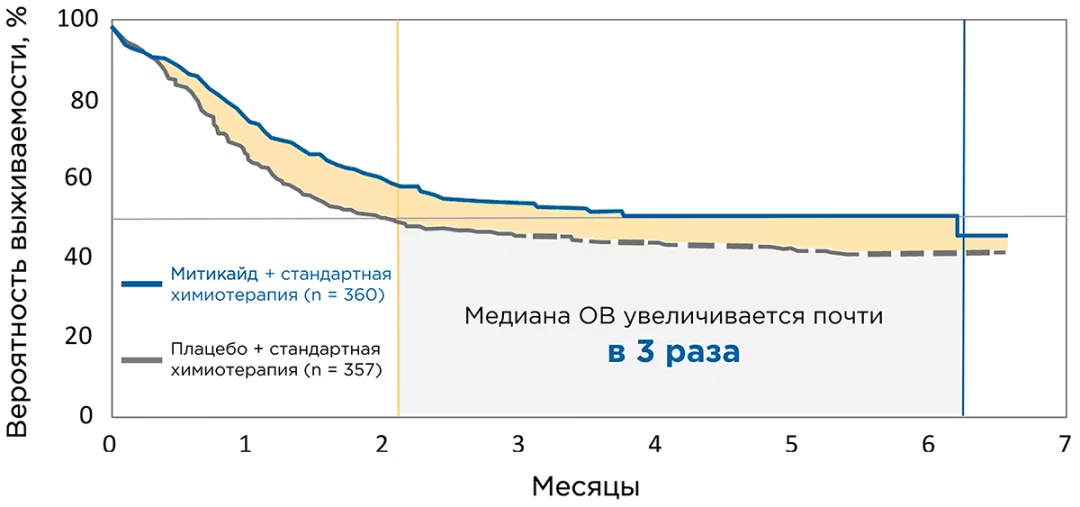
Рисунок 1. Эффективность мидостаурина в исследовании RATIFY
Список литературы
- Острые миелоидные лейкозы. Клинические рекомендации Ассоциации онкологов России и Национального гематологического общества. (2020).
- Döhner H. et al. Diagnosis and management of AML in adults: 2017 ELN recommendations from an international expert panel. Blood 129, (2017).
- Heuser M. et al. Acute myeloid leukaemia in adult patients: ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-up. Annals of Oncology 31, (2020).
- Bertoli S. et al. Time from diagnosis to intensive chemotherapy initiation does not adversely impact the outcome of patients with acute myeloid leukemia. Blood 121, (2013).
- https://www.nccn.org/professionals/physician_gls/pdf/aml.pdf. Acute Myeloid Leukemia. National Comprehensive Cancer Network (NCCN) Guidelines. (2020).
- Stone R.M. et al. Midostaurin plus Chemotherapy for Acute Myeloid Leukemia with a FLT3 Mutation. New England Journal of Medicine 377, (2017).
11213592/RYD/WEB/07.24/0