エンレスト 臨床データ
オルメサルタン対照二重盲検比較試験(国内第Ⅲ相臨床試験)
エンレストはオルメサルタンに比べ、収縮期血圧のベースラインからの変化量を有意に低下し、オルメサルタン20mgに対するエンレスト200mgの非劣性が確認され、優越性が検証されました
最終評価時の平均座位収縮期血圧(msSBP)変化量〔主要評価項目〕
および平均座位拡張期血圧(msDBP)変化量〔副次評価項目〕(FAS)
(オルメサルタン20mg群とエンレスト200mg群におけるmsSBP変化量の群間比較のみ検証的な解析結果)
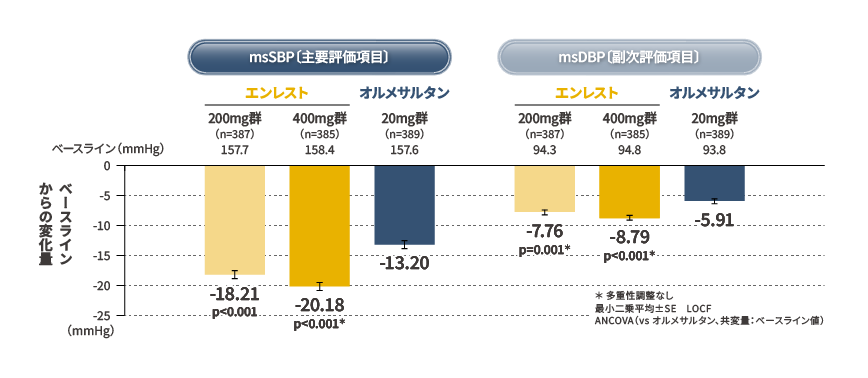
| 【非劣性の確認】 投与群間差(エンレスト200mg群-オルメサルタン20mg群)の最小二乗平均:-5.01mmHg〔95%信頼区間:-6.949,-3.061〕(非劣性限界値:2mmHg) |
社内資料:日本人高血圧患者におけるエンレストのオルメサルタンに対する優越性検証試験(国内第Ⅲ相試験、A1306試験)[承認時評価資料]
Rakugi H, et al.: Hypertens Res. 2022; 45(5): 824-833
[利益相反]本研究はノバルティスから資金提供を受けました。著者のうち4名はノバルティスの社員です。その他にノバルティスからコンサルティング料、講演料等の報酬を受領した著者が含まれます。
オルメサルタン対照二重盲検比較試験(国内第Ⅲ相臨床試験)
24時間自由行動下血圧測定(ABPM※)による24時間平均収縮期血圧のベースラインからの変化量は、エンレストの投与によりオルメサルタンに比べ有意に低下しました
※Ambulatory Blood Pressure Monitoring
最終評価時(8週時)におけるABPMによる24時間平均収縮期血圧(maSBP)変化量〔副次評価項目〕(FAS)
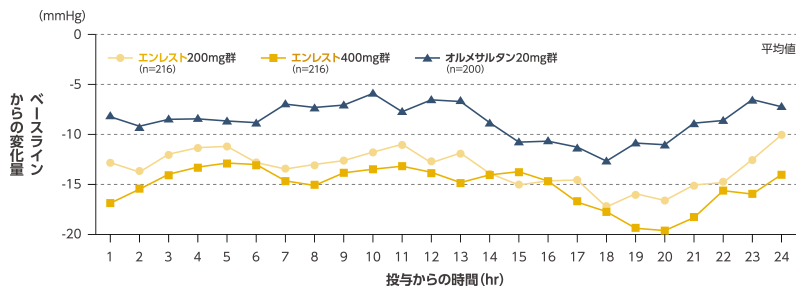
最終評価時の24時間maSBPのベースラインからの変化量は、エンレスト200mg群で-13.44mmHg、400mg群で-14.99mmHgであり、オルメサルタン20mg群の-8.78mmHgと比較し、いずれも有意に低下した(多重性調整なし:p<0.001、反復測定ANCOVA、共変量:ベースライン値、要因:投与群、投与後時間および投与群と投与後時間との交互作用)。
最終評価時(8週時)のABPMによる平均収縮期血圧(maSBP)変化量の24時間推移(FAS)
社内資料:日本人高血圧患者におけるエンレストのオルメサルタンに対する優越性検証試験(国内第Ⅲ相試験、A1306試験)[承認時評価資料]
オルメサルタン対照二重盲検比較試験(国内第Ⅲ相臨床試験)
エンレスト群ではオルメサルタン群に比べ、有意に高い収縮期および拡張期血圧のレスポンダー率※1が示されました
また、「高血圧治療ガイドライン2019」の降圧目標に注目したレスポンダー率※2は下図の通りでした
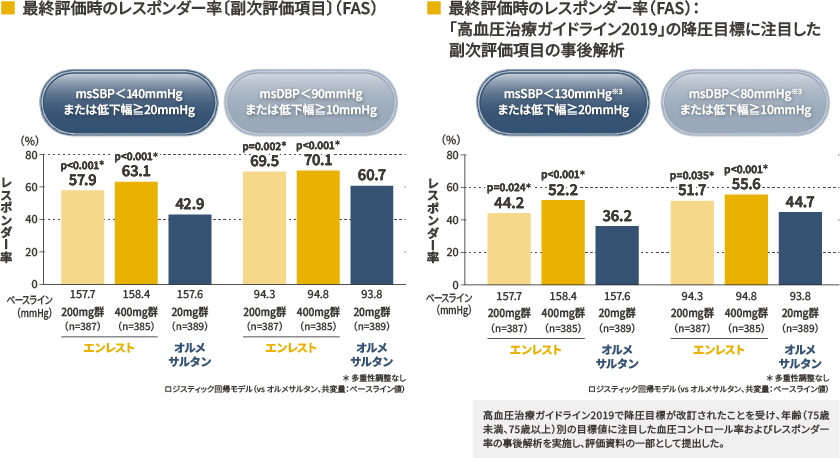
※1: 平均座位収縮期血圧(msSBP)<140mmHg または低下幅≧20mmHg となった患者の割合および平均座位拡張期血圧(msDBP)<90mmHg または低下幅≧10mmHg となった患者の割合
※2: 平均座位収縮期血圧(msSBP)<130mmHg または低下幅≧20mmHg となった患者の割合および平均座位拡張期血圧(msDBP)<80mmHg または低下幅≧10mmHg となった患者の割合
※3: 75歳以上の場合は、msSBP<140mmHg、msDBP<90mmHg
社内資料:日本人高血圧患者におけるエンレストのオルメサルタンに対する優越性検証試験(国内第Ⅲ相試験、A1306試験)[承認時評価資料]
Rakugi H, et al.: Hypertens Res. 2022; 45(5): 824-833
[利益相反]本研究はノバルティスから資金提供を受けました。著者のうち4名はノバルティスの社員です。その他にノバルティスからコンサルティング料、講演料等の報酬を受領した著者が含まれます。
オルメサルタン対照二重盲検比較試験(国内第Ⅲ相臨床試験)
副作用発現率は、エンレスト200mg群4.7%、同400mg群4.4%、オルメサルタン群4.4%でした
副作用の発現状況(SAF)
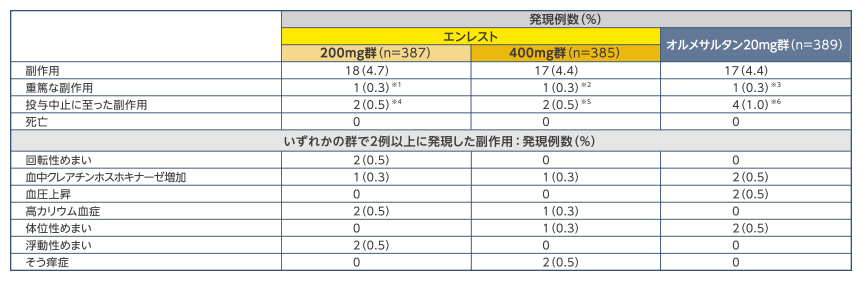
SAF:ランダム化された被験者のうち治療期に治験薬を1回以上投与されたすべての被験者
※1:くも膜下出血1例 ※2:肝胆道系疾患1例 ※3:白内障1例 ※4:便秘、胃炎、悪心、くも膜下出血、各1例(便秘、胃炎、悪心は同一症例に発現) ※5:肝胆道系疾患、そう痒症、各1例 ※6:高血圧、不安定血圧、血圧上昇、血管浮腫、蕁麻疹、各1例(血管浮腫、蕁麻疹は同一症例に発現)
社内資料:日本人高血圧患者におけるエンレストのオルメサルタンに対する優越性検証試験(国内第Ⅲ相試験、A1306試験)[承認時評価資料]
Rakugi H, et al.: Hypertens Res. 2022; 45(5): 824-833
[利益相反]本研究はノバルティスから資金提供を受けました。著者のうち4名はノバルティスの社員です。その他にノバルティスからコンサルティング料、講演料等の報酬を受領した著者が含まれます。
オルメサルタン対照二重盲検比較試験(国内第Ⅲ相臨床試験)
試験デザイン:目的、対象、方法
エンレストの効能又は効果に関連する注意において、「過度な血圧低下のおそれ等があり、原則として本剤を高血圧治療の第一選択薬としないこと。」とされているので、ご留意ください。
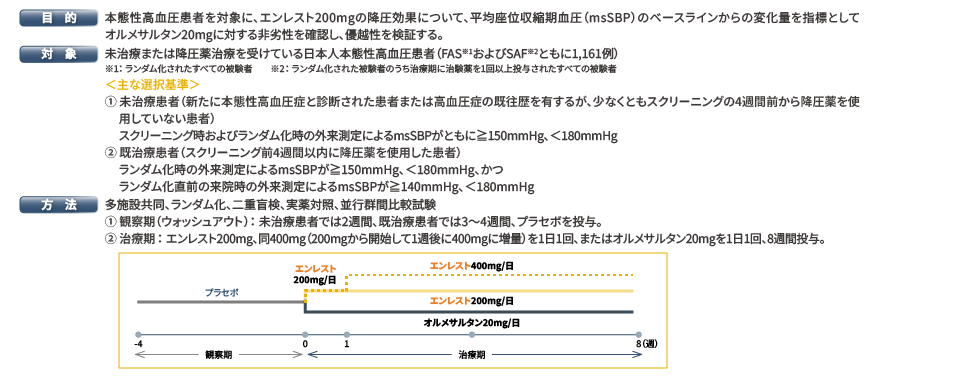
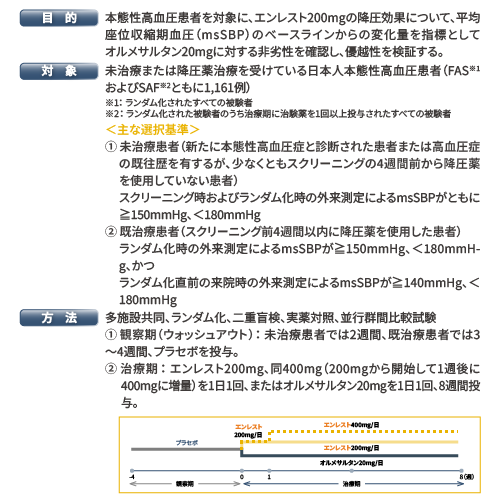
| オルメサルタンの用法及び用量 通常、成人にはオルメサルタン メドキソミルとして10~20mgを1日1回経口投与する。なお、1日5~10mgから投与を開始し、年齢、症状により適宜増減するが、1日最大投与量は40mgまでとする。 |
| 【5. 効能又は効果に関連する注意(抜粋)】 <高血圧症> 5.5 過度な血圧低下のおそれ等があり、原則として本剤を高血圧治療の第一選択薬としないこと。 |
社内資料:日本人高血圧患者におけるエンレストのオルメサルタンに対する優越性検証試験(国内第Ⅲ相試験、A1306試験)[承認時評価資料]
Rakugi H, et al.: Hypertens Res. 2022; 45(5): 824-833
[利益相反]本研究はノバルティスから資金提供を受けました。著者のうち4名はノバルティスの社員です。その他にノバルティスからコンサルティング料、講演料等の報酬を受領した著者が含まれます。
オルメサルタン対照二重盲検比較試験(国内第Ⅲ相臨床試験)
試験デザイン:評価項目、解析計画、事後解析

社内資料:日本人高血圧患者におけるエンレストのオルメサルタンに対する優越性検証試験(国内第Ⅲ相試験、A1306試験)[承認時評価資料]
Rakugi H, et al.: Hypertens Res. 2022; 45(5): 824-833
[利益相反]本研究はノバルティスから資金提供を受けました。著者のうち4名はノバルティスの社員です。その他にノバルティスからコンサルティング料、講演料等の報酬を受領した著者が含まれます。
オルメサルタン対照二重盲検比較試験(国内第Ⅲ相臨床試験)
患者背景(FAS)
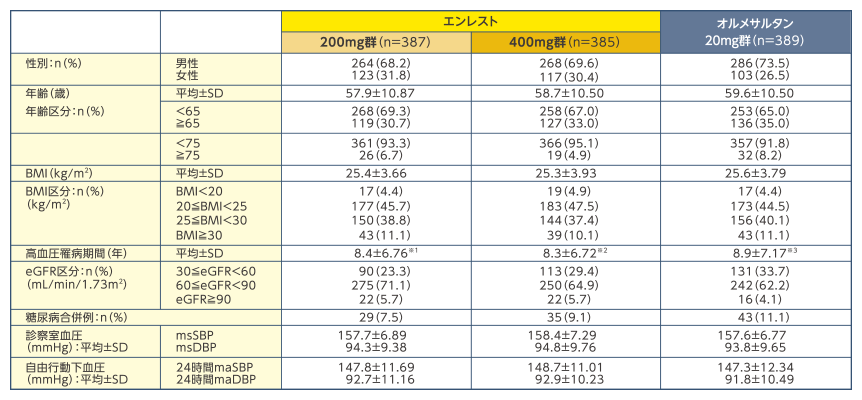
※1:n=386 ※2:n=384 ※3:n=388
BMI:body mass index、eGFR:推算糸球体濾過量、msSBP:平均座位収縮期血圧、msDBP:平均座位拡張期血圧、maSBP:自由行動下測定による平均収縮期血圧、maDBP:自由行動下測定による平均拡張期血圧、SD:標準偏差
社内資料:日本人高血圧患者におけるエンレストのオルメサルタンに対する優越性検証試験(国内第Ⅲ相試験、A1306試験)[承認時評価資料]
Rakugi H, et al.: Hypertens Res. 2022; 45(5): 824-833
[利益相反]本研究はノバルティスから資金提供を受けました。著者のうち4名はノバルティスの社員です。その他にノバルティスからコンサルティング料、講演料等の報酬を受領した著者が含まれます。