En el CM avanzado RH+ HER2- KISQALI (ribociclib) + TE* puede beneficiar a sus pacientes con metástasis viscerales y características agresivas de la enfermedad1,2
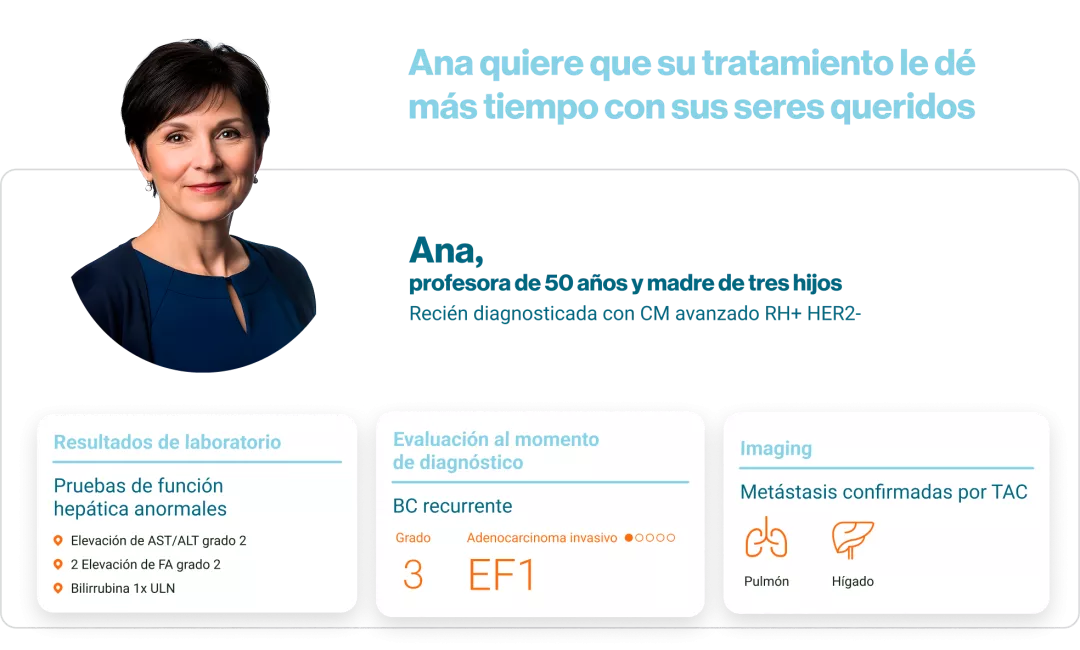
CMA: Cáncer de mama avanzado; RH+: receptores hormonales positivos; HER2-: receptor 2 del factor de crecimiento epidérmico humano negativo; AST: aspartato aminotransferasa; ALT: alanina aminotransferasa; FA: fosfatasa alcalina; ULN: límite superior de la normalidad, por sus siglas en inglés; ECOG: Eastern Cooperative Oncology Group; EF: estado funcional; TAC: tomografía axial computarizada.
¿Cómo puedes ayudar a Anna a conseguir su objetivo?
KISQALI® + TE* en 1L aumentó el beneficio de la mSG frente a la TE sola1
Análisis agrupado de MONALEESA† | mSG con una media de seguimiento de 72 meses.1,3

Incluyendo IA y fulvestrant.1 † Análisis combinado de 1124 pacientes con metástasis viscerales (incluyendo metástasis hepática o ≥3 sitios de enfermedad) de los estudios MONALEESA. 714 de estas pacientes recibieron tratamiento de 1L y están incluidas aquí (395 pacientes recibieron KISQALI® + TE). Estos datos son exploratorios y sólo se han utilizado para generar una hipótesis.1 ‡ HR = 0.79; IC de 95%: 0.65–0.97; p=0.023.
Aumento de 1 año en la mSG con KISQALI® + TE frente a TE sola.‡1
Elija KISQALI para ayudar a mejorar los resultados de sus pacientes con enfermedad agresiva, incluidos aquellos con metástasis viscerales1,2
MONALEESA-2: N-668, doble ciego. controlado con placebo, 1.1 aleatorizado, multicéntrico, ensayo de fase III en mujeres poetmenopáusicas con HR+/HER2- aBC. Como 1L en enfermedad avanzada. Sin tratamiento endocrino previo para el CBa y sin quimioterapia sistémica previa para la enfermedad avanzada. KISQALI 600 mg o placebo por vía oral una vez al día (3 semanas sí/1 semana no)+ Al (Ie trozol 2,5 mg continuo). El criterio de valoración primario fue la SLP evaluada localmente y el criterio de valoración secundario clave fue la SG. Otros criterios secundarios de valoración fueron la RRO (respuesta completa o parcial), la RCE (respuesta global más enfermedad estable durante 24 semanas o más), la seguridad y las evaluaciones de la calidad de vida*.
MONALEESA-3: N-726, doble ciego. controlado con placebo, aleatorizado 2:1, ensayo de fase Ill. Como 1L y 2L en enfermedad avanzada más aquellas con recaída temprana en mujeres postmenopáusicas con CBa HR+/H ER2-. KISQ ALI 600 mg o placebo por vía oral una vez al día (3 semanas on/1 vyeek off)+ 500 mg de fulvestrant intramuscular. El criterio de valoración primario fue la SLP evaluada localmente. Los criterios secundarios de valoración fueron la SG, la RRO, la RBC y la seguridad y tolerabilidad. 1L se definió como: pacientes con CBa recién diagnosticada (de novo) o pacientes con recaída >12 meses desde la finalización de la TE (neo)adyuvante sin tratamiento para CBa o enfermedad metastásica.
MONALEESA-7: N=672, doble ciego, controlado con placebo, aleatorizado 1:1, ensayo de fase III en mujeres pre o perimenopáusicas con CBa HR+/HER2-. Como d o s i s única en enfermedad avanzada y en pacientes que recibieron una o menos líneas de quimioterapia para el CBa. KISQALI 600 mg o placebo por vía oral una vez al día f3 semanas on/1 semana off)+ Al (letrozol 2,5 mg o anastrozol 1mg) o tamoxifeno" 2O mg por vía oral una vez al día de forma continua+ agonista de la LHRH (goserelina 3,6 mg por vía subcutánea el día 1de cada ciclo). El criterio de valoración principal fue la SLP evaluada por el investigador. El criterio de valoración secundario clave fue la SG, definida como
el tiempo transcurrido desde la aleatorización hasta la muerte por cualquier causa.'
KISOALI no debe administrarse conjuntamente con tamoxifeno.
Abreviaturas:1L, primera línea, 2L, segunda línea, ABC, cáncer de mama avanzado, IA, inhibidor de la aromatasa; ALP, fosfatasa alcalina; ALT. alanina transaminasa; AST, aspartamo aminotransferasa: CBR, tasa de beneficio clínico, Cl, intervalo de confianza; Combo CT; quimioterapia combinada: TC. tomografía computerizada: DFI, intervalo libre de enfermedad; ECOG PS. Estado funcional del Eastern Cooperative Oncology Group: RE+: receptor de estrógenos positivo; TE: terapia endocrina; HER2: factor de crecimiento epidérmico humano 2 negativo; HR: hazard ratio. HR+. receptor hormonal positivo; HRQoL. calidad de vida relacionada con la salud; LFT: pruebas de función hepática; mBC: cáncer de mama metastásico; mOS: mediana de supervivencia global; mPFS: mediana de supervivencia libre de progresión. ORR, tasa de respuesta global; SG, supervivencia global; SLP, supervivencia sin progresión: TFR. tFP¿ttFñent failure rate; TTF, time to treatment f¿tilure; TTR, time to
response; ULN, límite superior de la normalidad.
References:
Yardley DA. et al. Ann Oncol. 2022;33(S7).S629.
Lu Y-S. et al. J Clin Oncol 2024: JCO24OO144. doi.1O.1200/JCO.24.00144.
Yardley DA, et al. Presentación P205P. Presentado en la Sociedad Europea de Oncología Médica 2022. 9-13 septiembre. París. Francia.
Hortobagyi GN, et al. N Engl J Med. 2022;386l1O}:942—950.
Neven P. et al. Breast Cancer Res. 2O23:25.103.
Lu Y-S, et al. Clin Cancer Res. 2022;28:851-8S9.
Hortobagyi GN, et al. N Engl J Med. 2016;375(18):1738—1748.
Blamon DJ, et at. J Clin Oncol. 2018:36T24):2465—2472.
KISQALI. Resumen de las características del producto.
Haga clic aquí para consultar el Resumen de las características del producto KISOALI. IIrisc i t link tc KI SMALI Sm F'C]
Consulte el Resumen de las Características del Producto antes de prescribir KISQALI.
KISQALI está indicado para el tratamiento de mujeres con cáncer de mama localmente avanzado o metastásico positivo para receptores hormonales (RH) y negativo para el receptor 2 del factor de crecimiento epidérmico humano (HER2), en combinación con un inhibidor de la aromatasa o un inhibidor de la aromatasa.
fulvestrant como tratamiento endocrino inicial, o en mujeres que hayan recibido tratamiento endocrino previo.9
En mujeres pre o perimenopáusicas, el tratamiento endocrino debe combinarse con un agonista de la hormona liberadora de hormona luteinizante (LHRH).9
Notificación de acontecimientos adversos: |

