iDFS - iDFS por compromiso ganglionar - OS - Perfil de seguridad - Conclusiones

continúa reduciendo el riesgo de recurrencia más allá de los 3 años de ventana de tratamiento, soportando su uso como terapia adyuvante en pacientes con cáncer de mama RH+/HER2- con un alto riesgo de recurrencia, incluyendo pacientes N0 de alto riesgo.
iDFS en la población ITT
Abreviaturas:
IANE: Inhibidor de aromatasa no esteroideo. iDFS: sobrevida libre de enfermedad invasiva, por sus siglas en inglés. ITT: población con intención a tratar, por sus siglas en inglés.

El beneficio en iDFS también es consistente en el análisis de subgrupos, destacando la diferenciación por compromiso ganglionar:
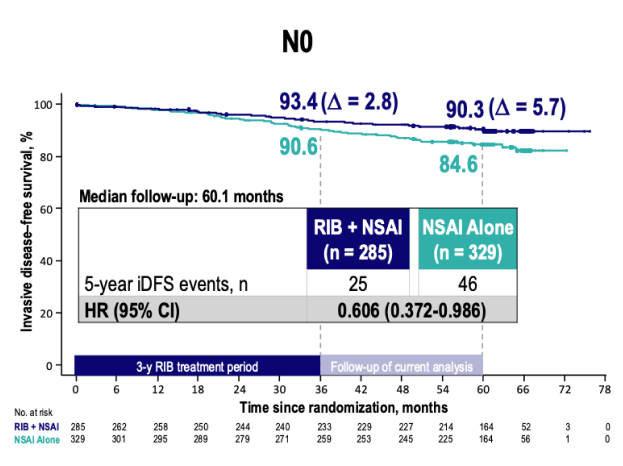
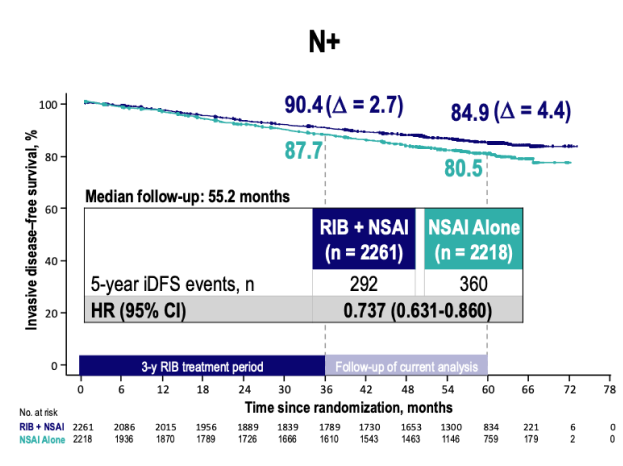
Abreviaturas:
RIB: ribociclib. NSAI: inhibidor de aromatasa no esteroideo, por sus siglas en inglés.

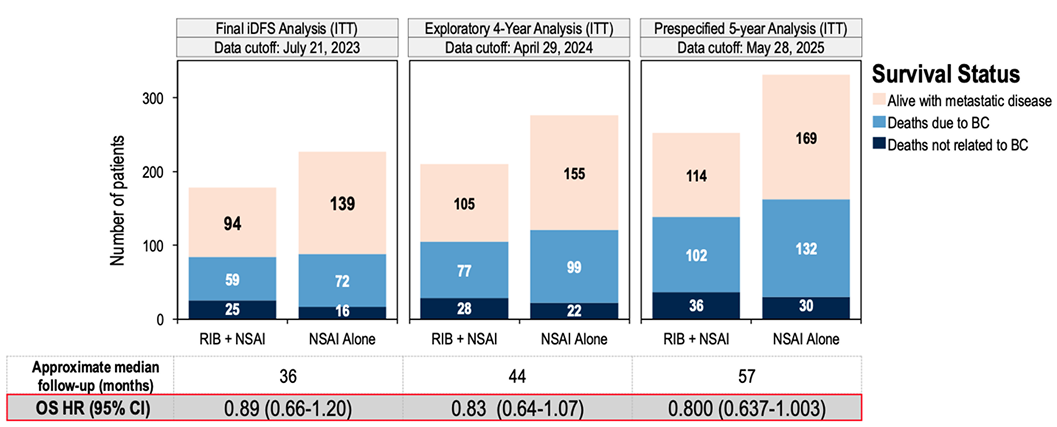
A medida que maduran los datos de sobrevida global (OS), se mantiene una tendencia positiva a favor de ribociclib + IANE
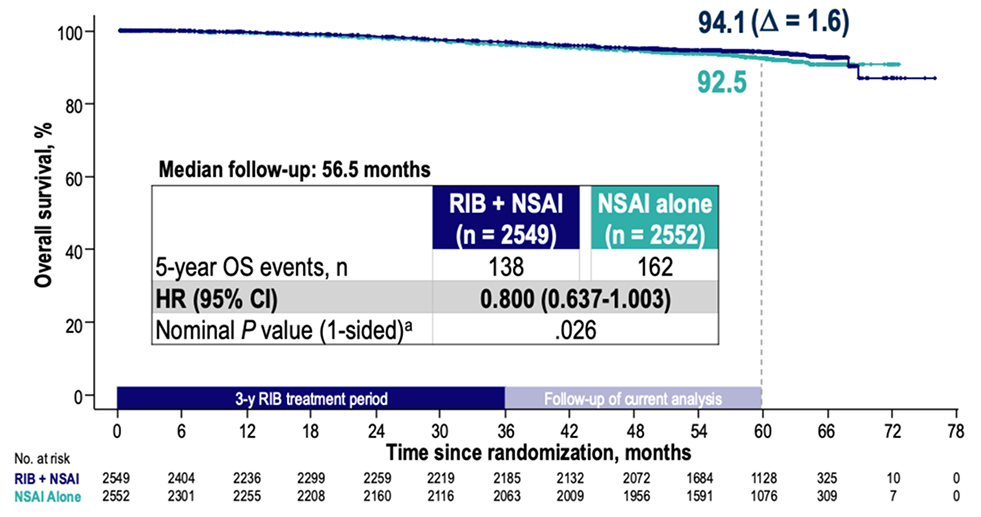
Abreviaturas:
Overall Survival: Sobrevida Global.
Estado de supervivencia a lo largo del tiempo:
Menor mortalidad relacionada con cáncer de mama en el brazo de ribociclib

The incidence of adverse events has remained stable. The most common all grade AEs in the ribociclib plus NSAI arm were neutropenia, arthralgia, and nausea.
Liver-related AEswere predominantly alanine aminotransferase or aspartate aminotransferase elevations without concomitant bilirubin increase.
27.2% required a ribociclib dose reduction with the primary reason being Aes (582 patients [23.0%]).
Early discontinuation due to AEs occurred in 509 patients (20.0%) in the ribociclib plusNSAI arm, representing a less than 1% increase from the protocol specified final iDFS analysis (498 patients [19.5%]).
Conclusiones

Referencias:
1. Crown J, Stroyakovskii D, Yardley DA, Huang C-S, Fasching PA, Bardia A, Chia S, Im S-A, Martín M, Xu B, Barrios CH, Untch M, Moroose R, Hurvitz SA, Hortobagyi GN, Slamon DJ, Visco F, Spera G, Li Z, Loi S. Adjuvant ribociclib plus nonsteroidal aromatase inhibitor therapy in patients with HR+/HER2− early breast cancer: NATALEE 5-year outcomes. ESMO Congress 2025; Berlin, Germany.
2. Slamon D, Lipatov O, Nowecki Z, McAndrew N, Kukielka‑Budny B, Stroyakovskiy D, et al. Ribociclib plus Endocrine Therapy in Early Breast Cancer. N Engl J Med. 2024 Mar 21;390(12):1080–91. doi: 10.1056/NEJMoa2305488.
Novartis de Colombia S.A. Calle 93B No. 16-31. PBX 654 44 44. Bogotá, D.C. Novartis de Colombia S.A. Novartis Pharma, AG de Basilea, Suiza ® = Marca registrada. Fecha de aprobación: XX/oct/2025; Fecha de Caducidad: XX/oct/2027; ID del contenido: FA-XXXXXXX. Material dirigido a médicos. Más información en el Departamento Médico de Novartis S.A Colombia: 6544444 o al correo [email protected]. Si desea reportar un evento adverso ingrese al siguiente link: www.novartis.com/report. Este material no es promocional en lenguaje, apariencia o intención. Si se hace alusión a productos o indicaciones no aprobados por la autoridad regulatoria del país, será bajo el estricto propósito educativo, de genuino intercambio científico y para incluir las alternativas de tratamiento de forma balanceada, completa y vigente. Este material no pretende sustituir o reemplazar una decisión clínica ni terapéutica. Ribociclib (un inhibidor de quinasas dependientes de ciclinas iCDK4/6), está indicado para el tratamiento de mujeres pre, peri o post menopaúsicas y varones con cáncer de mama avanzado o metastásico con positividad de receptores hormonales (RH) y negatividad de receptores 2 del factor de crecimiento epidérmico humano (HER2) en combinación con: • Inhibidor de aromatasa como tratamiento inicial de base endocrina. • Fulvestrant, como tratamiento inicial de base endocrina o luego de presentar progresión de la enfermedad después de terapia endocrina. • En varones y en mujeres pre o perimenopáusicas, la hormonoterapia debe combinarse con un agonista de la hormona liberadora de la hormona luteinizante (LHRH, por sus siglas en inglés). Actualmente, Ribociclib no cuenta con aprobación por la agencia regulatoria local de Colombia para uso en pacientes con cáncer de mama RH+HER2- estadio II o III. No se autoriza la grabación, toma de fotografías y distribución del material y tampoco difusión por medios no autorizados por Novartis.

