

Klinische Studien zu LEQVIO® im Überblick
Die Studien ORION-9, -10 und -11 waren multizentrische, doppelblinde, randomisierte, placebokontrollierte, 18-monatige Studien. Etwa 3’600 Patienten wurden randomisiert, um entweder Placebo oder LEQVIO® 284 mg zusätzlich zu einer maximal verträglichen Statindosis mit oder ohne weitere lipidsenkende Therapie zu erhalten. Die Patienten erhielten eine Anfangsdosis von LEQVIO® oder Placebo als subkutane Injektion, dann eine weitere nach 3 Monaten und danach weitere Gaben alle 6 Monate.1
- Prozentuale Veränderung des LDL-C-Wertes nach 17 Monaten gegenüber dem Ausgangswert im Vergleich zu Placebo und im zeitlichen Mittel
- Prozentuale Veränderung des LDL-C-Wertes im Zeitraum zwischen 3 Monaten und 18 Monaten gegenüber dem Ausgangswert im Vergleich zu Placebo1
Gepoolte Analyse von 3'660 Patienten: bislang grösster gepoolter Datensatz für LEQVIO®1

Studiendesign der LEQVIO®-Studien ORION-9, ORION-10 und ORION-11
† Typ-2-Diabetes, FH oder ein 10-Jahres-Risiko für ein kardiovaskuläres Ereignis von ≥ 20 %, bewertet durch den Framingham Risk Score für kardiovaskuläre
Erkrankungen
Gepoolte Analyse von LEQVIO®-Studien bei Patienten mit familiärer Hypercholesterinämie oder Atherosklerose1
Hintergründe zur Studie

Atherosklerotische kardiovaskuläre Erkrankungen (ASCVD)4
- Herz-Kreislauf-Erkrankungen sind die häufigste Todesursache nicht nur weltweit, sondern auch in der Schweiz.4,5
- Langfristige LDL-C-Exposition ist ein wichtiger Prädiktor für das Risiko atherosklerotischer Herz-Kreislauf-Erkrankungen.4

Familiäre Hypercholesterinämie2
- Genetische Störung(en), gekennzeichnet durch erhöhtes LDL-C von Geburt an und erhöhtes Risiko für Atherosklerose und vorzeitige CV-Ereignisse.
- Heterozygoter (HeFH) oder homozygoter (HoFH) Genotyp.

Prävention und aktuelle Behandlungsbeschränkungen
- Bei 4 von 5 Patienten mit sehr hohem Risiko reichen die derzeitigen lipidsenkenden Therapien allein nicht aus, um die empfohlene LDL-C-Zielewerte zu erreichen.6

LEQVIO® (Inclisiran)2,3
- LEQVIO® ist eine doppelsträngige small-interfering RNA, die die Produktion des Enzyms Proprotein Convertase Subtilisin/Kexin Type 9 (PCSK9) in der Leber hemmt.
- Dadurch kommt es zu einer erhöhten Anzahl von LDL-Rezeptoren an der Oberfläche der Hepatozyten und einer verbesserten Aufnahme von LDL-Partikeln in die Leber, wodurch der Blutspiegel des LDL-C gesenkt wird.
- Dies führt zu einer anhaltenden Senkung des LDL-C bei zweimaliger jährlicher Verabreichung.
Ziel der Studie1

Das Ziel dieser Studie war es, eine gepoolte Analyse auf Patientenebene aus 3 Phase-III-Studien von Inclisiran durchzuführen: ORION-9, -10 and -11

Koprimäre Endpunkte
Prozentuale Veränderung der LDL-C-Spiegel von Baseline bis Tag 510.1
Zeitbereinigte prozentuale Veränderung der LDL-C-Spiegel von Baseline nach Tag 90 und Tag 540.1

Wichtige sekundäre Endpunkte
- Absolute Veränderung des LDL-C von Baseline bis Tag 510.1
- Zeitbereinigte absolute Veränderung des LDL-C von Baseline zwischen Tag 90 und Tag 510.1
- Prozentuale Veränderung von Baseline bis Tag 510 in in PCSK9, TC, ApoB und Non-HDL-C1
- Sicherheits- und Verträglichkeitsprofil von Inclisiran, gemessen durch UE, SUE, Vitalparameter und klinische Laborwerte1
Gemeinsame Einschluss- und Ausschlusskriterien der Studien ORION-9, ORION-10 und ORION-111
Haupteinschlusskriterien der ORION-Studien 9, 10 und 11-3
Hauptausschlusskriterien der ORION-Studien 9, 10 und 12,3
Studiendesign1
Studienteilnehmer mit heterozygoter familiärer Hypercholesterinämie* (ORION-9), atherosklerotischer kardiovaskulärer Erkrankung (ASCVD**) (ORION-10) oder ASCVD** und ASCVD-Risikoäquivalenten*** (ORION-11), die eine maximal verträgliche Statintherapie mit oder ohne andere LDL-C-senkende Mittel einnahmen, wurden im Verhältnis 1:1 randomisiert.
Die Studienteilnehmer haben entweder LEQVIO® oder Placebo erhalten, verabreicht durch subkutane Injektion an Tag 1, Tag 90 und danach alle 6 Monate für 540 Tage.
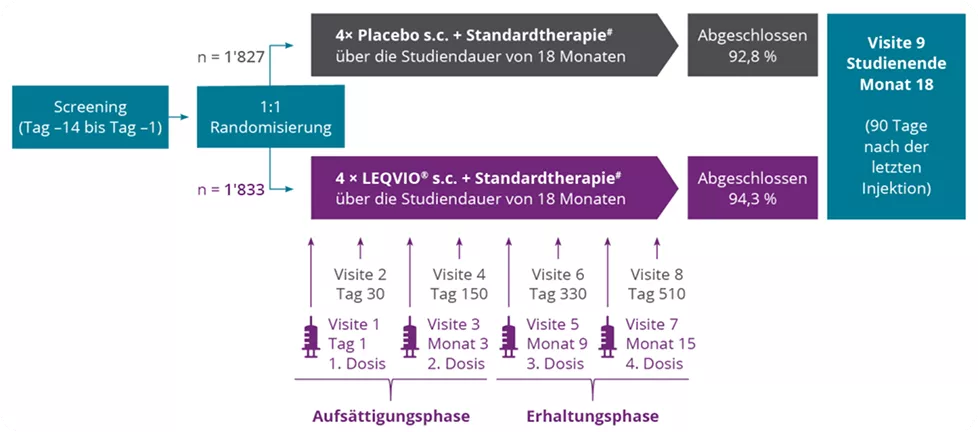
* Heterozygote familiäre Hypercholesterinämie: HeFH in der Familie; LDL-C ≥ 100 mg/dl.
** Atherosklerotische kardiovaskuläre Erkrankung: diagnostizierte ASCVD (KHK, HKE, pAVK); LDL-C ≥ 70 mg/dl.
*** Risikoäquivalente der atherosklerotischen kardiovaskulären Erkrankung: ASCVD-Risikoäquivalente (Typ-2-Diabetes, FH,10-Jahres-Risiko > 20 %); LDL-C ≥ 70 mg/dl bei Patienten mit ASCVD oder ≥ 100 mg/dl bei Patienten mit ASCVD-Risikoäquivalent.
# Die Patienten beider Studiengruppen wurden mit einem maximal verträglichen Statin behandelt.
Ergebnisse1
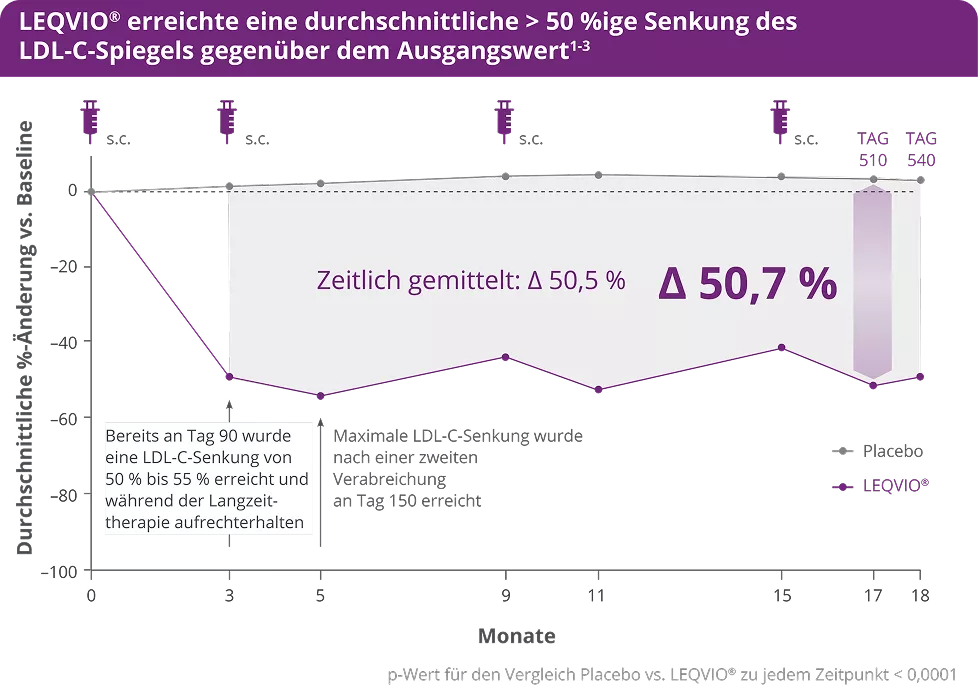
Senkung des LDL-C-Spiegels gegenüber dem Ausgangswert
Mehr Patienten erreichten die vordefinierten LDL-C-Werte mit LEQVIO® im Vergleich zu Placebo1
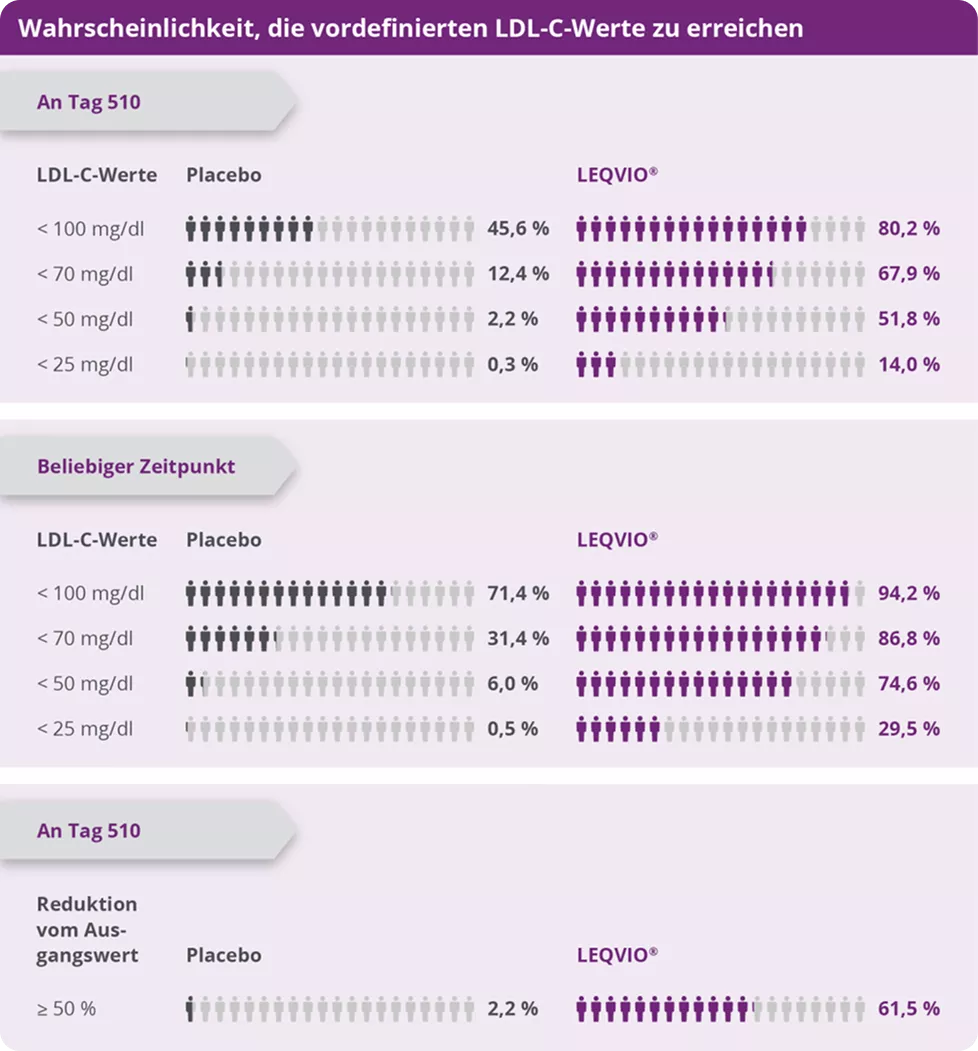
Reduktion des LDL-C-Wertes unter LEQVIO® zu unterschiedlichen Zeitpunkten
Zusammenfassung und klinische Implikationen1

* Ab der 2. Injektion.
** Sicherheitsprofil für insgesamt 3’655 Patienten, mit einer Exposition von ca. 2'653 Personenjahren von LEQVIO®.
# Typ-2-Diabetes, FH oder ein 10-Jahres-Risiko für ein kardiovaskuläres Ereignis von ≥ 20 %.
Laden Sie sich die Zusammenfassung der gepoolten Analyse zur klinischen Studien als PDF herunter oder lesen Sie hier die originale gepoolte Analyse ORION-9/10/11 .
Sie möchten mehr erfahren?
Entdecken Sie hier mehr Wissenswertes über LEQVIO®
ASCVD: atherosklerotische Herz-Kreislauf-Erkrankungen; CKD: chronischen Niereninsuffizienz; CV: kardiovaskulär; EAS: Europäische Gesellschaft für Atherosklerose; ECS: Europäische Gesellschaft für Kardiologie; eGFR: geschätzte glomeruläre Filtrationsrate; FH: familiäre Hypercholesterinämie; HK: Herzkrankheit; LDL-C: Low Densitiy Lipoprotein Cholesterin; PCSK9: Proproteinkonvertase Subtilisin/Kexin Typ 9
Kurzfachinformation Leqvio®
▼ Dieses Arzneimittel unterliegt einer zusätzlichen Überwachung. Für weitere Informationen siehe Fachinformation/Patienteninformation LEQVIO® auf www.swissmedicinfo.ch.
Abgabekategorie: B
Referenzen
- Wright, R.S., et al., Pooled Patient-Level Analysis of Inclisiran Trials in Patients with Familial Hypercholesterolemia or Atherosclerosis. J Am Coll Cardiol, 2021. 77(9):p. 1182–93. doi: 10.1016/j.jacc.2020.12.058.
- Raal, F.J., et al., Inclisiran for the Treatment of Heterozygous Familial Hypercholesterolemia. N Engl J Med, 2020. 382(16): p. 1520–30. doi: 10.1056/NEJMoa1913805.
- Ray, K.K., et al., Two Phase 3 Trials of Inclisiran in Patients with Elevated LDL Cholesterol. N Engl J Med, 2020. 382(16): p. 1507–19. doi: 10.1056/NEJMoa1912387.
- Ference, B.A., et al., Low-density lipoproteins cause atherosclerotic cardiovascular disease. 1. Evidence from genetic, epidemiologic, and clinical studies. A consensus statement from the European Atherosclerosis Society Consensus Panel. Eur Heart J, 2017. 38(32): p. 2459–72. doi: 10.1093/eurheartj/ehx144.
- BAG Schweiz, Todesursachen Statisik 2022, https://www.bfs.admin.ch/bfs/de/home/statistiken/gesundheit/gesundheitszustand/sterblichkeit-todesursachen/spezifische.html, zuletzt aufgerufen im Juni 2023.
- Vrablik M et al. Lipid-lowering therapy use in primary and secondary care in Central and Eastern Europe: DA VINCI observational study. Atherosclerosis, 2021;Oct 2021(334):66 – 75.





